乳腺癌五年生存率逐年上升,最新的治疗因素都在这了!
通过手术进行根治性切除仍是结直肠癌的主要治疗方法,当然根据患者的自身差异性,医生也会制定个性化的手术治疗方案。
多数早期患者可以通过根治性切除达到痊愈,中晚期患者通过手术结合辅助化、放疗等手段,也可获得较好结果。
本期的“大咖谈全程,常筑新希望”专家采访,我们到了邀请山东省立医院保健外科主任、胃肠外科副主任刘洪俊教授,为我们分享结直肠癌全程管理中的手术治疗相关的问题。
对于全国人民来说,我们在即将战胜“新冠疫情”的曙光中送走了农历庚子年。
有人说,你不送走,它也会走。或许送走它最好的方式,就是每个中国人努力奋斗的方式。大家努力的方式其实只有一个,那就是活下来。尽力地活下来,本身就是送走每一种困难的方式。
对每个乳腺癌患者来说,过去的那一年里更是雪上加霜、荆棘遍布的一年。
2021年1月初,世界卫生组织国际癌症研究机构(IARC)发布了2020年全球最新癌症负担数据。统计显示,2020年,女性乳腺癌首次超过肺癌,成为全球最常见癌症,约占新发癌症病例的11.7%[1]。
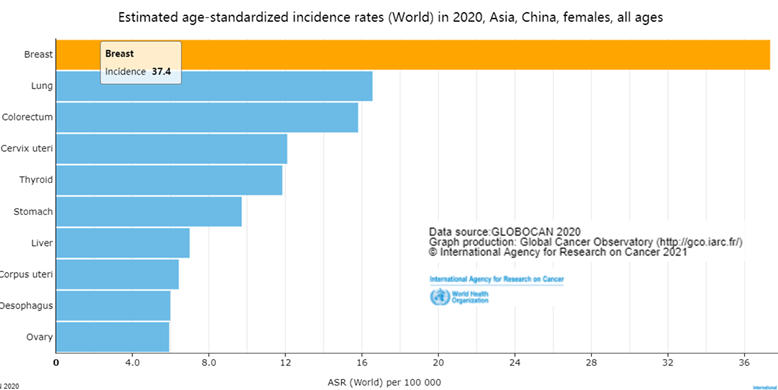
在新确诊的患者中,每8名就有1名是乳腺癌患者。其次分别是肺癌、结直肠癌、前列腺癌、胃癌、肝癌、宫颈癌、食管癌、甲状腺癌和膀胱癌。
虽然如此,在女性之中,乳腺癌并不是致死率最高的癌症。我国的数据显示,2020年,约有300万中国人因癌症而死亡,乳腺癌的死亡病例数排在第四位,在肺癌、结直肠癌、胃癌之后。这一状况的形成,其实与乳腺癌诊疗水平的逐年提高密不可分,目前乳腺癌的5年生存率已高达90%,远超其他癌种,中国乳腺癌患者5年生存率高达83.2%,在过去10年间提高了7.3%[2]。
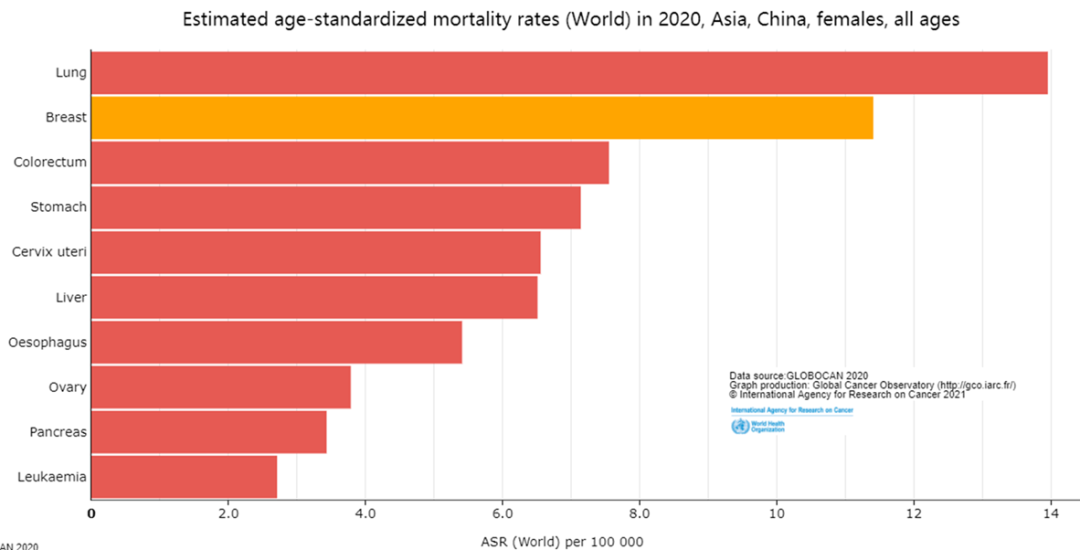
在对抗癌症的这场“战争”中,虽然各种“不确定性”给我们带来种种恐惧,但我们依然在幸存的夹缝中看到了数不清的进步!
这期“前沿资讯”,小觅蜂将用三篇“前沿资讯”和大家盘点一下,在“百感交集”却逐渐远去的2020,乳腺癌治疗领域发生着哪些你还不怎么了解的变化。这些变化即将在新的一年里改变我们每个人的一生!
今天是第一篇:为了让乳腺癌在手术前实现“完全缓解”,我们在新辅助治疗这个领域都有哪些值得铭记的关键时刻!
早期HER2阳性乳腺癌新辅助:
心脏毒性较大的蒽环类用药方案正被取代
近年来,随着对乳腺癌发病机制的研究越来越深入,乳腺癌的精准靶向治疗已“渐入佳境”,逐渐从晚期扩展到早期,从术后扩展到术前。目前,新的化疗-靶向组合治疗方式正在让乳腺癌患者的总体生存周期逼近普通人群,而治疗期间所遭的“罪”也正变得越来越小。
去年,对于HER2阳性乳腺癌患者来说,最值得我们关注的进步是新的靶向组合方式正在逐步取代造成严重心脏负担的蒽环类药物。
方式一
术后靶向方案也可以在术前使用
对于早期乳腺癌,标准的治疗方案是在手术后使用多西他赛(T)+卡铂(Cb)+曲妥珠单抗(H)辅助治疗,简称TCH辅助化疗。
近年来,一项多中心临床研究通过长达10年的随访,发现这一方案同样适用于术前新辅助治疗。和传统的“多柔比星+环磷酰胺,序贯多西他赛+曲妥珠单抗”方案(EC-TH)相比,新方案能够明显延缓复发,延长患者寿命[3]。
更关键的是,由于新方案调整了治疗药物和治疗方式,对患者心脏造成的负担明显减少了!有心脏并发症的患者有机会利用新辅助化疗更好的融入日常生活。
2020年,ASCO(美国临床肿瘤学会)会议公布的另一项研究,再次证实了新方案在术前新辅助治疗的价值。
“
研究发现,TCH方案能让一半以上的患者通过术前化疗让肿块“消失”(pCR),进一步保障了手术的有效性。与此相对的,旧方案仅能让不到40%的患者实现这一目标[4]。
”
方式二
“妥妥双靶”走向术前
“妥妥双靶”是乳腺癌靶向治疗领域的又一个“里程碑事件”,科学家们在品类众多的HER2靶向药中寻到了曲妥珠单抗的一类“姊妹药”——帕妥珠单抗,能够很好的解决曲妥珠单抗耐药的问题。
但是,既往这种组合用药方案几乎仅用于近年来也被用于晚期或早期患者的术后辅助,有没有可能通过术前“新辅助”的方式,给早期乳腺癌患者提供更多“保障”呢?
2020年,有两项高质量的临床研究证实了“妥妥双靶”在术前全身治疗中表现非凡!
“
第一项研究的多年随访数据发现,在不使用蒽环类药物的前提下,通过联合化疗、曲妥珠单抗、帕妥珠单抗,患者手术成功实现肿瘤“消失”(pCR)的几率明显提升了!患者的复发风险、生存周期也明显增加了[5]。
”
我们知道,曲妥珠单抗本身具有一定程度的心脏毒性,这种多靶向药治疗方式由于去除了蒽环类药物的影响,整体上并没有造成更多的心脏疾病风险。
作为激素受体(HR)阳性、HER2阳性的早期乳腺癌一直是乳腺癌治疗领域的“宠儿”,因为我们有多种药物可以选择。由于内分泌药物不能与化疗同时使用,对于有新辅助化疗指征的患者就不得不面临一个“两难”——术前阶段选择靶向+化疗好?还是靶向+内分泌更好?
“
另一项前瞻性研究帮我们解决了这个问题,结果显示,双靶联合化疗组患者的pCR率明显高于双靶联合内分泌(56.8% ∶ 23.9%),前者使超过一半的患者实现了肿瘤的完整“去除”(pCR),后者只有23%[6]。
”
看来,对于激素依赖型HER2阳性乳腺癌,双靶联合化疗的新辅助疗法更具优势!
关于“妥妥双靶”,小觅蜂在早前的报道中做过详细论述,感兴趣的觅友可以点击查看晚期转移一定要放弃吗?“妥妥双靶”告诉你答案
早期Luminal乳腺癌:
术前化疗解锁新方案
一般临床上把三阴型的乳腺癌视为一种高危乳腺癌,也就是指激素受体(ER/PR)阴性、HER2阴性;相应的,如果是HER2阳性乳腺癌,在多种HER2靶向药的加持下,患者的远期生存数据显然更好。
可说到最后,还有一种介于“三阴”和HER2阳性之间的乳腺癌没提到,那就是激素受体阳性、HER2阴性的所谓“Luminal”乳腺癌。术前阶段,目前指南的首选推荐就是“紫杉类+蒽环类+环磷酰胺”21天一周期的化疗。次选就是新辅助内分泌疗法。
但这方面的研究还不够深入,肿瘤专家也没有给予比较强的推荐共识。
虽然缺少更好的用药选择,于是肿瘤专家们在用药周期上打起了主意。尤其是在摸清了乳腺癌细胞的生长规律以后,部分专家建议将间隔21天的用药流程缩短到14天。这种用药模式已进入CSCO指南的推荐当中,用于HER2阴性早期患者的术后治疗。
2020年,欧洲肿瘤内科学会( ESMO)会议公布了该研究47个月的随访结果,认为这一方案对HER2阳性和三阴的乳腺癌均不适用这种新辅助方案,唯独Luminal型乳腺癌效果良好[7]!

早期三阴乳腺癌新辅助:
联合免疫治疗让三阴患者摆脱“无可救药”旧局面
最后,小觅蜂再和大家聊一聊三阴乳腺癌。早期乳腺癌中近两成患者是三阴型的[9],即雌激素受体(ER)阴性、孕激素受体阴性(PR)以及HER2阴性。
无论是单抗还是多种小分子靶向药,HER2阳性乳腺癌的治疗选择很多,效果也很不错。可是HER-2阴性,尤其是三阴性患者,化疗以外几乎无药可选。
三阴患者术前的首选方案是依旧是化疗方案,年纪较轻的三阴患者,特别是携带BRCA突变的乳腺癌,因为对铂类特别敏感,可以在术前使用含铂方案。
总的来说,从远期的复发、转移进展等方面看,三阴性肿瘤和HER2阳性肿瘤仍旧是也不可同日而语的。
上帝关上了一道门就会打开一扇窗。在几乎没有任何创新疗法可用的同时,免疫治疗的兴起似乎正给三阴乳腺癌患者内心的“阴霾”投来一束光。虽然乳腺癌本身并不属于免疫原性较强的肿瘤[8],可是三阴型似乎是个例外。
“
在较早的KEYNOTE-522研究中就发现,三阴乳腺癌术前治疗体系加用PD-1抑制剂能提高肿瘤“完全缓解”(pCR)的几率!但这项研究的对照数据不足尚不足以改变三阴治疗的体系。
去年进行的另一项三期临床研究,使用了一种经典的PD-L1抑制剂作为免疫治疗药物。研究发现,“免疫+化疗”的治疗方式能使术前缓解率(pCR)达到57.6%!相比之下,单一化疗仅能实现41.1%[10]。
”
记得年前的时候,小觅蜂和大家讨论的乳腺癌疫苗,许多觅友一直在问“什么时候能用上”?详细文章可点击右方,乳腺癌疫苗重大突破,患者五年无病生存率高达100%
这个“用上”似乎成为阻碍乳腺癌彻底治愈的最后一道“门槛”。
幸运的是,随着化疗、靶向治疗、内分泌、免疫等多种优化组合方式的出现,乳腺癌这一最高发的癌症正在一点一点的“被攻克”,更多好的治疗方式正在一步一步的“被用上”。
新辅助治疗作为早期患者手术成功、长期生存的“保险杠”,一直以来受到乳腺癌研究的重视,在“难上加难”的2020,我们依然看到一大批新 · 新辅助疗法“横空出世”,将会给大家将来的生活添加更多保障!
除了新辅助,还有哪些值得大家关注的2020乳腺癌最新进展呢?我们会在接下来的两篇文章中继续探讨,期待你的持续关注!
乳腺癌互助圈
乳腺癌互助圈
每日向您发送关于乳腺癌预防科普、治疗日记以及术后恢复的知识。呵护女性健康,给您一个和谐幸福的家!
905篇原创内容
公众号
封面图片来源:稿定设计
责任编辑:乳腺癌互助君
参考资料
[1] Global Cancer Observatory: December, 2020
[2] ALLEMANI C, MATSUDA T, DI CARLO V, et al. Global surveillance of trends in cancer survival 2000-14(CONCORD-3): analysis of individual records for 37 513 025 patients diagnosed with one of 18 cancers from 322 population-based registries in 71 countries[J]. Lancet, 2018, 391(10125):1023-1075.
[3] SLAMON D, EIERMANN W, ROBERT N, et al. Abstract S5- 04: Ten year follow-up of BCIRG-006 comparing doxorubicin plus cyclophosphamide followed by docetaxel(AC→T) with doxorubicin plus cyclophosphamide followed by docetaxel and trastuzumab(AC→TH) with docetaxel, carboplatin and trastuzumab(TCH) in HER2 + early breast cancer[J]. Cancer Res, 2016, 76(4 Supplement):S5-04-S05-04.
[4] GAO H F, WU Z, LIN Y, et al. Neoadjuvant TCH(docetaxel/ darboplatin/trastuzumab) versus EC-TH(epirubicin/ cyclophosphamide followed by docetaxel/ trastuzumab ) in patients with HER2-positive breast cancer(neoCARH): A randomised, open-label, multicenter, phase Ⅱ trial[J]. J Clin Oncol, 2020, 38(15_suppl):585.
[5] RAMSHORST M S V, VOORT A V D, WERKHOVEN E V, et al. Three-year follow-up of neoadjuvant chemotherapy with or without anthracyclines in the presence of dual HER2-blockade for HER2-positive breast cancer(TRAIN-2): A randomized phase Ⅲ trial[J]. J Clin Oncol, 2020, 38(15_suppl):501.
[6] GLUZ O, NITZ U, CHRISTGEN M, et al. De-escalated chemotherapy versus endocrine therapy plus pertuzumab + trastuzumab for HR + /HER2 + early breast cancer(BC): First efficacy results from the neoadjuvant WSG-TP-II study[J]. J Clin Oncol, 2020, 38(15_suppl):515
[7] SCHNEEWEISS A, MÖBUS V, TESCH H, et al. 160O Survival analysis of the randomized phase Ⅲ GeparOcto trial comparing neoadjuvant chemotherapy(NACT) of iddEPC versus weekly paclitaxel, liposomal doxorubicin(plus carboplatin in triple-negative breast cancer, TNBC)(PM(Cb)) for patients(pts) with high-risk early breast cancer(BC)[J]. Ann Oncol, 2020, 31:S303-S304
[8] TOPALIAN S L, DRAKE C G, PARDOLL D M. Immune checkpoint blockade: a common denominator approach to cancer therapy[J]. Cancer Cell, 2015, 27(4):450-461.
[9] PETKOV V I, MILLER D P, HOWLADER N, et al. Breastcancer-specific mortality in patients treated based on the 21- gene assay: a SEER population-based study[J]. NPJ Breast Cancer, 2016, 2:16017.
[10] HARBECK N, ZHANG H, BARRIOS C H, et al. LBA11 IMpassion031: Results from a phase Ⅲ study of neoadjuvant(neoadj) atezolizumab + chemotherapy in early triple-negative breast cancer(TNBC)[J]. Ann Oncol, 2020, 31:S1144
[11] 翟婧彤, 吕丹, 马飞., 2020年度乳腺癌治疗新进展., 肿瘤综合治疗电子杂志[J], 2021年第1期24-33,共10页., 中国医学科学院医学与健康科技创新工程协同创新团队项目(2017-I2M-3-004)