KEYNOTE药物系列研究梳理
近年来,肿瘤治疗已逐渐进入精准免疫治疗时代。帕博利珠单抗作为 PD-1 单抗的先行者,在非小细胞肺癌(NSCLC)中用一系列研究诠释了「获益人群全覆盖,活得久才是硬道理」。
KEYNOTE-024[1]-改写 NSCLC 治疗格局,优势人群去化疗
KEYNOTE-024 是一项全球多中心、随机对照Ⅲ期临床研究,旨在评估帕博利珠单抗对比含铂化疗治疗 PD-L1 TPS ≥ 50%、无表皮生长因子受体(EGFR)、间变性淋巴瘤激酶(ALK)驱动基因突变的晚期 NSCLC 初治患者的有效性与安全性。2020 年欧洲肿瘤内科学会(ESMO)KEYNOTE-024 研究的 5 年总生存(OS)公布,重塑了 NSCLC 治疗格局。
研究纳入了 16 个国家的 305 例患者,1:1 随机分为帕博利珠单抗单药治疗组(200 mg Q3W)及化疗组。
化疗组患者疾病进展后可交叉至帕博利珠单抗治疗组。研究的主要终点为无进展生存(PFS),次要终点为 OS、客观缓解率(ORR)及安全性。尽管化疗组中近 66% 的患者接受后续 PD-1/PD-L1 抑制剂治疗(化疗组 55% 的患者交叉至帕博利珠单抗治疗),帕博利珠单抗组 5 年 OS 率较化疗组提升近一倍(31.9% 对 16.3%),中位 OS 分别为 26.3(28.3-40.4)个月对 13.4(9.4-18.3)个月,HR 0.62(95% CI,0.48-0.81)(图 1)。
帕博利珠单抗单药组中,39 例患者完成了 2 年 35 周期的治疗,其 ORR 高达 82%[32/81,4 例完全缓解(CR),28 例部分缓解(PR)],3 年 OS 率高达 81%。同时治疗相关不良反应帕博利珠单抗组明显低于化疗组(76.6% 对 90%),长期随访并未发现新的不良反应。
KEYNOTE-024 是第一个报道晚期 NSCLC 一线免疫治疗 5 年疗效的 III 期研究,经过 5 年随访继续支持了帕博利珠单抗是 PD-L1 TPS ≥ 50% 晚期 NSCLC 患者的有效一线治疗方案。
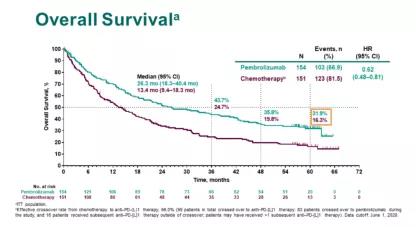
图 1 KEYNOTE-024 OS 曲线
KEYNOTE-042[2]-扩大免疫治疗获益人群至 TPS ≥ 1%
KEYNOTE-042 是一项全球、随机、开放标签Ⅲ期临床研究。入组 PD-L1 TPS 评分 ≥ 1% 的 EGFR 突变阴性或 ALK 重排阴性局部晚期或转移性 NSCLC 患者初治患者,对比了帕博利珠单抗单药和含铂双药化疗。
1274 例患者随机按 1∶1 分配接受帕博利珠单抗 200 mg 治疗或研究者选择的化疗方案(卡铂联合紫杉醇或培美曲塞),Q3W。所有患者治疗直至影像学进展、不可耐受的毒性、研究者决定停止治疗或患者要求退出。帕博利珠单抗最多治疗 35 周期,化疗组最多治疗 6 个周期。分配接受培美曲塞化疗的非鳞 NSCLC 患者可以选择接受培美曲塞单药维持治疗。研究的主要终点为 PD-L1 TPS ≥ 50% 患者的 OS; 次要终点为 PD-L1 TPS ≥ 1% 患者的 OS、PD-L1 TPS ≥ 50% 和 ≥ 1% 患者的 PFS。
3 年随访数据显示 PD-L1 TPS ≥ 50% 患者中, 帕博利珠单抗和含铂化疗组的中位 OS 分别为 20 vs. 12.2 个月(HR = 0.68),3 年 OS 率分别为 31% vs. 18%;PD-L1 TPS ≥ 20% 患者中,以上数据分别为 18 vs. 13 个月(HR = 0.75) 和 28% vs. 19%;PD-L1 TPS ≥ 1% 患者中,以上数据分别为 16.4 vs. 12.1(HR = 0.80) 和 25% vs. 17%。
再次证实 Pembro 可改善所有人群(PD-L1 TPS ≥ 50%、TPS ≥ 20%、TPS ≥ 1%)的 OS(图 2),且具有可控的安全性。亚组分析,与 Keynote-024 研究结果一致的是 ≥ 50% 表达组患者疗效更佳,因此,很明显整体人群的生存获益是由 PD-L1 高表达组驱动的,而在 1-49% 表达亚组生存获益并不显著,提示部分患者并未从开始的 PD-1 治疗中获益。总生存曲线从开始出现了交叉,提示部分患者治疗前期不能真正获益并且面临疾病进展的风险,为联合治疗之路埋下伏笔。

图 2 KEYNOTE-042 预设亚组 OS 曲线
KEYNOTE-189[3]-首个获批的免疫联合化疗方案
KEYNOTE-189 研究是一项随机、对照、双盲Ⅲ期临床研究,入组 616 例初治的 EGFR 突变阴性或 ALK 阴性的晚期 NSCLC 患者,按 2:1 比例随机入组到帕博利珠单抗联合培美曲塞和铂类组(帕博利珠单抗 200 mg,每 3 周给药 1 次,连续 4 个周期),或安慰剂联合培美曲塞和铂类组。后续可使用帕博利珠单抗或安慰剂联合培美曲塞维持治疗,直至 35 个周期结束。对照组患者出现疾病进展,允许交叉至帕博利珠单抗联合化疗组接受治疗。以 OS 和 PFS 为双终点。
2018 年 4 月公布初期数据,并同步在线发表于《新英格兰医学杂志》。2020 年 ASCO 中位随访 31.0 个月的最终分析结果。两组中位 OS 分别为 22.0 个月(95%CI:19.5~24.5)和 10.6 个月(95%CI:8.7~13.6),与对照组相比试验组降低了 44% 的死亡风险(HR = 0.56,95%CI:0.46~0.69)(图 3)。两组 3 年的 OS 率分别为 31.3% 和 17.4%。
无论患者 PD-L1 表达如何,帕博利珠单抗联合化疗均带来了显著的 OS 获益。两组中位 PFS 为分别为 9.0 个月(95%CI:8.1~10.4)和 4.9 个月(95%CI:4.7~5.5)。帕博利珠单抗联合化疗组具有更高的客观缓解率(ORR:48.3% vs 19.9%。更加值得关注的是,在 56 例接受帕博利珠单抗联合化疗后完成 35 个周期帕博利珠单抗单药维持治疗的患者,其 ORR 高达 85.7%,包括 4 例完全缓解(CR),44 例部分缓解(PR)。探索性分析显示,不论患者基线时是否伴有肝转移或脑转移,帕博利珠单抗联合化疗相比安慰剂联合化疗,持续为患者带来 OS、PFS、ORR 的改善,同时不良反应易于管理。因此,帕博利珠单抗联合培美曲塞铂类在这部分患者中的一线标准治疗地位确立。
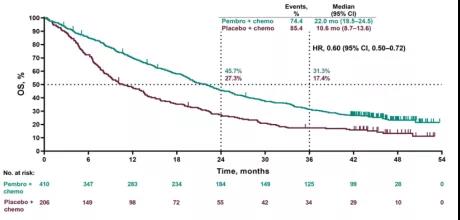
图 3 KEYNOTE-189 OS 曲线
KEYNOTE 407-晚期鳞癌患者新选择
KEYNOTE-407 研究是一项多中心、随机、双盲、安慰剂对照的 III 期临床研究,旨在评估帕博利珠单抗或安慰剂联合卡铂和紫杉醇/白蛋白紫杉醇用于 IV 期鳞状 NSCLC 患者一线治疗的疗效和安全性。符合入组条件的患者按 1:1 随机分组,接受帕博利珠单抗(200 mg)+化疗或安慰剂+化疗,Q3W,4 个周期,之后接受帕博利珠单抗或安慰剂维持治疗,最多 35 个周期。分层因素包括药物类型(紫杉醇或白蛋白结合型紫杉醇)、区域(东亚或其他地区)、PD-L1 表达水平。通过盲态孤立中央审查委员会评估,主要研究终点是 OS 和 PFS。共入组 559 例患者。
2021 ELCC 公布的最新结果显示,帕博利珠单抗联合化疗组的中位 OS 为 17.2 个月,对照组为 11.6 个月,HR 0.71(95%CI,0.59–0.86)(图 4);两组 3 年 OS 率分别为 29.7% 和 18.2%;中位 PFS2 分别为 13.8 个月和 9.1 个月,HR 0.59(95%CI,0.49–0.71)。在 55 例完成帕博利珠单抗 35 个周期的患者中,ORR 为 92.7%(5 例 CR,46 例 PR),其中 4 例患者(7.3%)SD。无论患者的 PD-L1 TPS 评分如何均可以从帕博利珠单抗联合化疗获益。此外,帕博利珠单抗联合化疗显示出可管理的安全性 [4]。
KEYNOTE-407 研究中国亚组(包括中国扩展队列)亚组共纳入 125 例患者 [5]。结果显示,帕博利珠单抗联合化疗组和化疗组中位 OS 分别为 17.3 个月 vs. 12.6 个月,联合组较化疗组降低了 56% 的死亡风险;联合组和化疗组中位 PFS 分别为 8.3 个月 vs. 4.2 个月,降低了 68% 的疾病进展或死亡风险;相比化疗组,联合组的 ORR 提升了 36.8%(ORR:78.5% vs. 41.7%)。35 例对照组患者交叉到帕博利珠单抗单药治疗,联合组仍有 31 例(48%)患者,化疗组仅有 4 例(7%)患者在继续接受治疗。值得一提的是,KEYNOTE-407 研究中在常规紫杉醇和白蛋白紫杉醇使用对比中发现,白蛋白紫杉醇取得了和常规紫杉醇相似的疗效,却降低了不良反应,最关键的一点是避免了常规紫杉醇激素的预处理。
因此,在转移性肺鳞癌的一线治疗上,帕博利珠单抗联合卡铂和紫杉类化疗相比于单纯化疗,无论患者接受哪种类型的紫杉类化疗,均可以显著改善 OS、PFS 和 ORR,患者均可以耐受。对于中国人群,帕博利珠单抗联合化疗一线治疗转移性鳞状 NSCLC 可以显著改善患者的 OS 和 PFS,且安全性可控。

图 4 KEYNOTE-407 OS 曲线
NSCLC 二线/后线治疗-KEYNOTE-010[6]
KEYNOTE-010 纳入 1024 例 PD-L1 肿瘤比例评分(TPS)≥ 1% 的经治晚期 NSCLC 患者,随机 1:1:1 接受帕博利珠单抗 2 mg/kg q3w、10 mg/kg q3w 或多西他赛 75 mg/m 2 q3w 治疗。免疫治疗持续 35 个周期(~2 年) 或直至疾病进展/不可接受的毒性,已完成 35 周治疗或 CR 后停药且治疗时间 ≥ 6 个月的患者,疾病进展后可以接受 17 个周期(1 年) 的第二阶段帕博利珠单抗治疗。
5 年随访数据结果显示 PD-L1 TPS ≥ 50% 患者的中位 OS 分别为 16.9 vs. 8.2 个月(HR = 0.55),5 年 OS 率 25.% vs. 8.2%;PD-L1 TPS ≥ 1% 患者的以上数据分别为 11.8 个月 vs. 8.4 个月(HR = 0.70) 以及 15.6% vs. 6.5%(图 5)。PD-L1 TPS ≥ 50% 患者的中位 PFS 为 5.3 vs. 4.2 个月(HR = 0.57),5 年 PFS 率分别为 18.2% vs. NR;PD-L1 TPS ≥ 1% 患者的以上数据分别为 4.0 vs. 4.1 个月(HR = 0.84) 以及 9.4% vs. 0.7%。79 例免疫组患者完成 35 周期(2 年) 治疗,ORR 为 98.7%(15 CR, 63 PR);其中 61 例(77.2%) 存活(38 例没有出现 PD);完成 35 周期(2 年) 治疗患者的 3 年 OS 率为 83.0%。
经过约 5 年的随访,与多西他赛相比,帕博利珠单抗单药二线/后线治疗为经治 PD-L1 TPS ≥ 1% 的晚期 NSCLC 患者的 OS 和 PFS 提供持续、有临床意义的改善,5 年 OS 率增加了一倍以上,15.6% 患者 5 年时依然生存;完成 35 个周期(2 年) 免疫治疗的患者获得持久缓解;2 年免疫治疗后疾病进展的大多数患者中,第二阶段的免疫治疗获得有意义的疾病控制。为二线治疗提供了新选择(FDA 获批)。
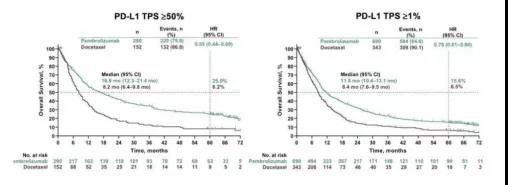
图 5 KEYNOTE-010 OS 曲线
帕博利珠单抗肺癌使用汇总
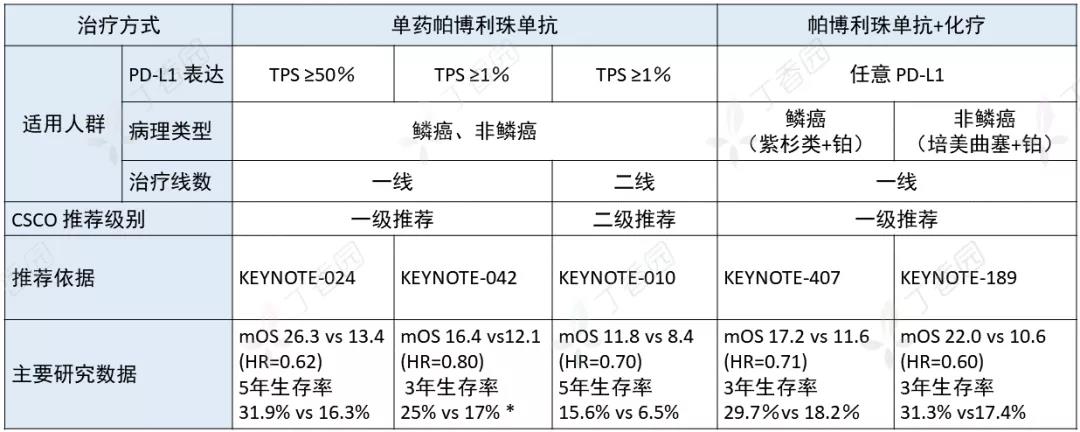
* 备注:对于 PD-L1 1%-49% 的人群,使用帕博利珠单抗单药和化疗疗效相当,但由于生存曲线存在交叉,提示对于化疗禁忌证患者,帕博利珠单抗单药可作为一种选择。