“铂应答” PARP抑制剂
卵巢癌被大家称为“沉默的致命物”,这是因为起病隐匿,且最初发病时症状不典型,故确诊时大多为晚期,且卵巢癌极易复发,患者3年复发率达70%左右,复发后治疗即使达到临床缓解,仍会复发,并且随着复发次数的增加,各种治疗的效果逐渐降低,并最终死于这一疾病。
在很多肿瘤提倡无化疗理念时,卵巢癌的铂类联合化疗方案依然是一线治疗的基础,所以含铂化疗的结果将直接影响后续治疗的选择。部分患者在一线治疗时既对铂类联合方案耐药,那么在后续治疗时,可考虑联合贝伐珠单抗等抗血管治疗药物;大多数患者初次使用含铂化疗方案后还是可以达到完全缓解(CR)或部分缓解(PR)的这些患者在完成一线治疗后,预后较好。并且随着PARP抑制剂的临床研究数据公布,这类患者通过后续的PARP抑制剂的维持治疗获益率更高。这些患者在后续的治疗时,就会有更多的治疗方案选择。
随着几个PARP抑制剂在我国获批用于含铂化疗应答的晚期卵巢癌患者一线维持、铂敏感复发维持治疗,PARP抑制剂用于维持治疗已成为卵巢癌治疗新模式,可显著延长患者铂类耐药的出现,为患者带来治疗新希望。
那哪些患者可以从PARP抑制剂获益呢?
人体中代谢活跃的细胞处于细胞周期的动态平衡中,而DNA的复制及修复机制是细胞存活的关键,不同的损伤因子对细胞造成损伤时,细胞修复机制就会启动,这其中包括DNA的修复机制。
人体内DNA损伤修复过程十分复杂,常见的包括PARP参与的DNA单链修复和BRCA等基因参与的双链修复(如:同源重组修复,HR)。当两种修复机制中的一种发生修复过程障碍时,细胞DNA可通过另一种方式进行修复,不会对细胞生存造成致死性影响。而当这两种DNA损伤修复能力都受到抑制时,则可能促进细胞的凋亡。PARP抑制剂的"合成致死"作用机制即是基于这种原理。在BRCA基因突变的肿瘤细胞中已经存在同源重组修复缺陷(HRD),此时再应用PARP抑制剂,就能同时抑制单链断裂的损伤修复,使细胞DNA无法通过这两个通路进行修复,进而促进肿瘤细胞的凋亡,发挥更强的抗肿瘤作用。
从“合成致死”的原理来看,PARP抑制剂可以在所有的HRD肿瘤细胞中发挥作用。BRCA1/2基因只是编码HR通路的关键组分之一,其中还涉及其他基因包括RAD51、ATM、MRE11、RPA和NBS1等,这些基因发生突变失活同样导致DNA双链损伤修复功能的缺陷,即HRD。
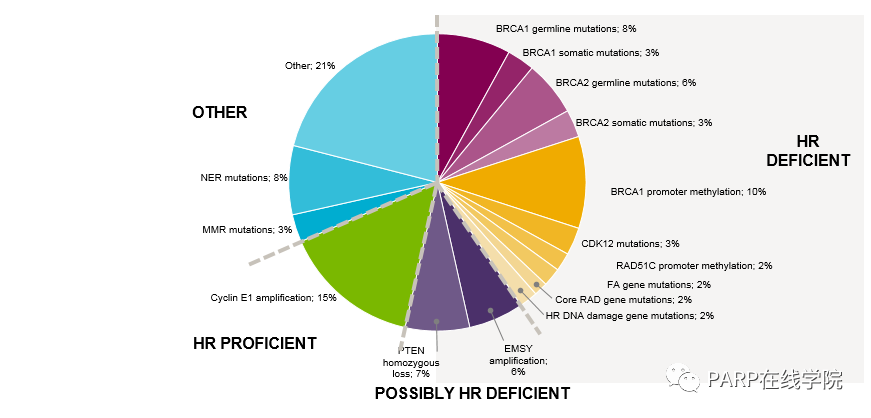
铂类化疗与PARP抑制剂存在相互协同作用。对于铂应答的肿瘤细胞,铂类化疗可能会造成DNA损伤。而如果DNA修复机制无法及时修复,肿瘤细胞就会发生致死性死亡。而PARP抑制剂可以阻碍损伤DNA的修复,这可能是PARP抑制剂对铂应答卵巢癌有效的原因之一。
在2009年发表于Lancet Oncology的一项I期临床研究显示, 接受奥拉帕利单药治疗(非维持治疗)携带BRCA突变的复发性卵巢癌患者, 获得CR/PR的比例与铂应答状态成正相关,患者对铂越敏感,反应率越高。也就是说,即使患者已经携带BRCA突变,对PARP抑制剂的疗效依旧与铂应答状态相关。
因此,铂类联合方案化疗有效的患者,再通过PARP抑制剂,可认为是“合成致死”机制的另一种组合形式。
既然铂应答的患者是PARP抑制剂的获益人群,铂应答患者在使用PARP抑制剂前还需要检测BRCA/HRD吗?
或许我们可以从以下研究中获得答案。
Study19研究入组了265例PSR卵巢癌患者,在≥2线铂类为基础的化疗达到CR或PR后,随机接受奥拉帕利或安慰剂维持治疗,研究结果显示,奥拉帕利组中位PFS达8.4个月,相比安慰剂组(4.8个月)延长了近2倍,疾病进展或死亡风险显著降低65%;亚组分析显示无论BRCA突变或BRCA野生型,PFS均显著延长;不仅如此,经过长达6年的长期随访数据显示,奥拉帕利可使患者长期生存获益,无论BRCA突变与否。
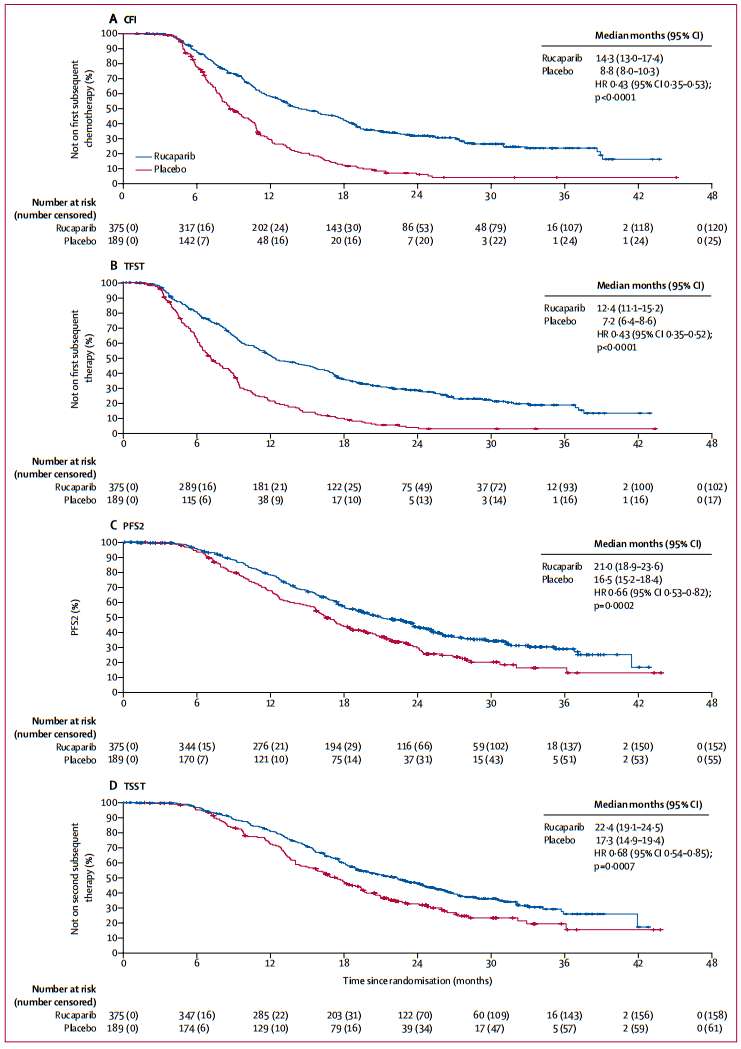
ARIEL3研究入组了564例PSR卵巢癌患者,在≥2线铂类为基础的化疗达到CR或PR后,随机接受卢卡帕利或安慰剂维持治疗,较安慰剂组mPFS延长了5.4个月(10.8个月对5.4个月),复发或死亡风险降低了64%(HR=0.36,95%CI: 0.30-0.45,P<0.0001)。通过对探索性进展后终点分析结果显示,在复发性卵巢癌患者进展后,卢卡帕利维持治疗具有持久的临床获益,接受卢卡帕利维持治疗患者的中位CFI、TFST、PFS2和TSST均显著长于安慰剂组,且无论突变状态如何,所有队列的探索性进展后终点均有临床获益。
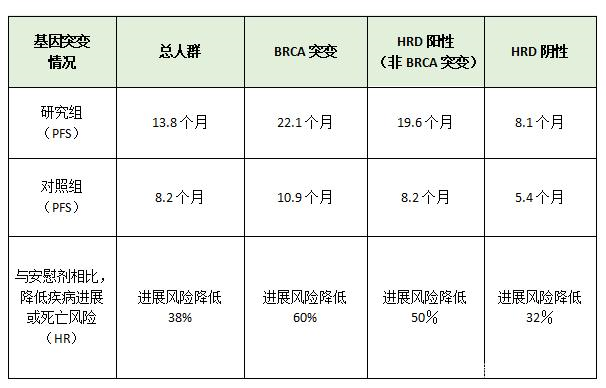
PRIMA研究入组了733例对一线含铂化疗应答的患者,其中也包括了此前一线卵巢癌研究中未被充分关注的那些疾病进展风险更高的患者。研究结果显示尼拉帕利在所有研究对象中与安慰剂相比可以降低38%疾病进展或死亡风险,无论是HRD阳性或是HRD阴性的患者都展示了有临床和统计学意义的临床获益。更是基于此研究,尼拉帕利获批用于含铂化疗应答的晚期卵巢癌患者一线维持治疗而无需考虑这些患者的生物标志物状态。
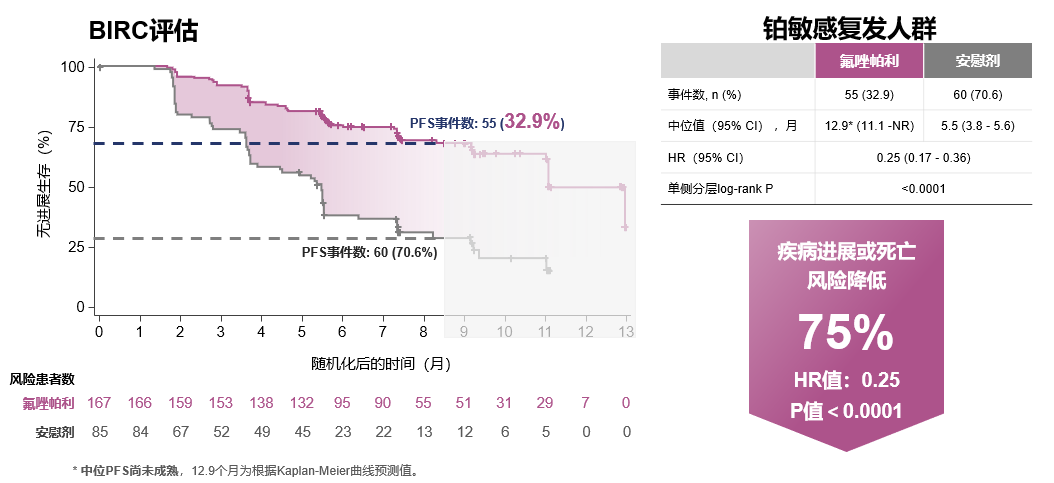
FZOCUS-2研究共入组了252例受试者。入组人群为既往接受过≥2线以铂为基础的化疗且CR或PR的患者。研究结果显示,相比安慰剂,氟唑帕利维持治疗能够显著延长铂敏感复发性卵巢癌患者的PFS,降低患者75%的疾病进展/死亡风险。且无论患者是否伴gBRCA1/2突变,均能从氟唑帕利治疗中获益。
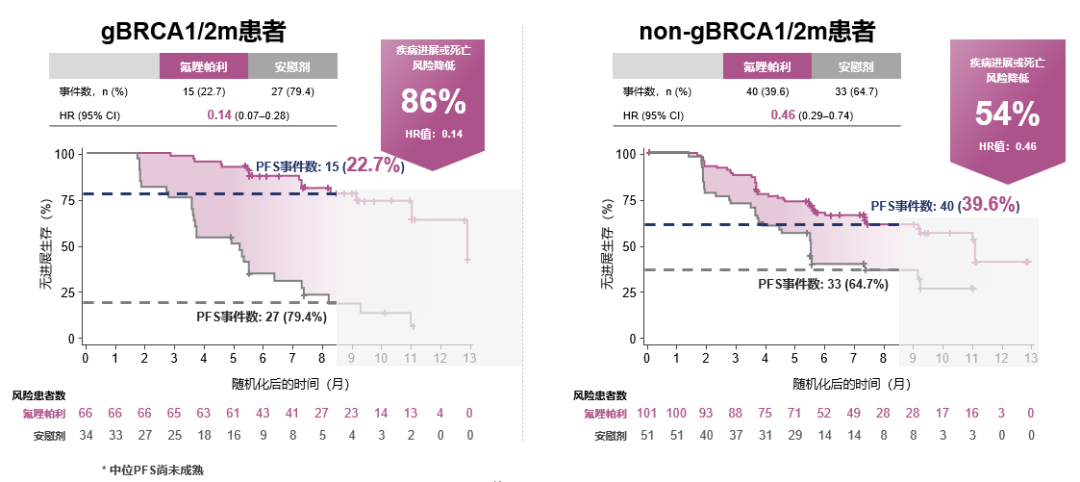
综合分析以上四个研究,我们不难发现:无论患者BRCA/HRD状态如何,只要是铂应答的患者,均可以从PARP抑制剂中获益。
同时,从近年的PARP抑制剂维持治疗临床研究来看,PARP抑制剂的应用已经逐渐从复发维持前移至一线维持、从BRCA突变人群扩大到一线铂应答人群。且一项纳入了三个随机对照试验的Meta分析结果表明,PARP抑制剂用于一线维持治疗,不论患者的BRCA/HRD状态如何,PARP抑制剂用于一线维持治疗相比安慰剂均可显著提升PFS。
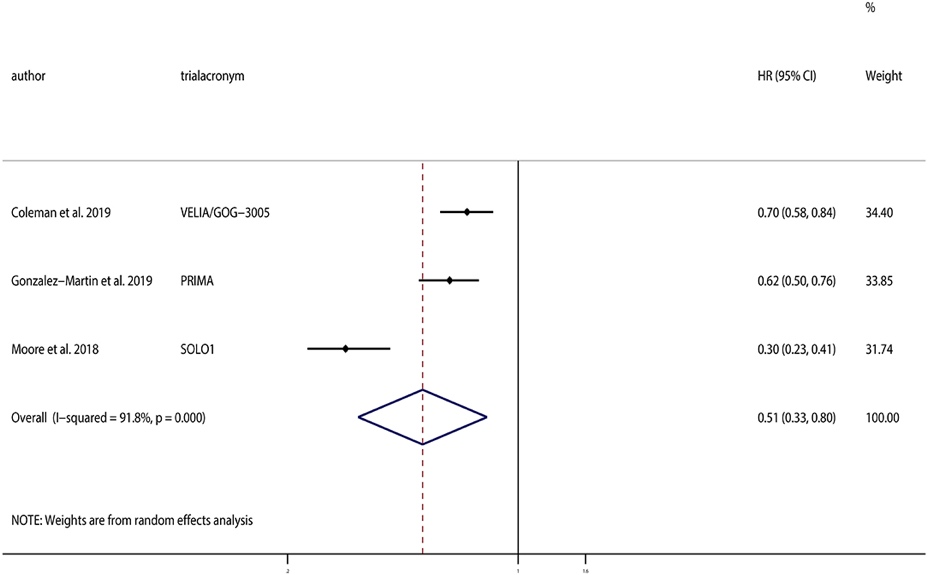
不论是从机制还是临床研究,我们都可以发现:无论患者BRCA/HRD状态如何,PARP抑制剂较安慰剂均可以显著延长铂应答患者的无进展生存期。且基于目前我国HRD检测尚无统一标准,铂应答状态可以是预测PARP抑制剂敏感性的指标,那么,铂应答的患者在使用PARP抑制剂前是否必须要检测BRCA/HRD呢?