免疫性反复流产
在妊娠状态下,母体产生的自身抗体和(或)自身反应性淋巴细胞以及某些细胞因子能攻击滋养层细胞、母-胎界面血管内皮细胞及胎儿细胞,影响胚胎的种植及其今后的生长发育,严重者可导致复发性流产、早产、胎儿生长迟缓、羊水过少、死胎、子痫前期/子痫、溶血、肝酶升高和低血小板综合征等不良妊娠结局,其中以复发性流产最为常见。
而与此同时,妊娠期雌激素水平上升,可激活体液免疫途径,使得原有自身免疫的活动度上升,病情进展,严重者可危及母婴生命安全。
抗磷脂综合征
诊断抗磷脂综合征的临床标准:
1.血管栓塞
任何器官或组织发生一次以上的动脉、静脉或小血管血栓,血栓必须被客观的影像学或组织学证实;组织学还必须证实血管壁附有血栓,但没有显著炎性反应;
2.病态妊娠
- 发生一次以上的在10周或10周以上不可解释的形态学正常的死胎,正常形态学的依据必须被超声或被直接检查所证实
- 在妊娠34周之前,因严重的子痫或子痫前期或严重的胎盘功能不全所致,1次以上的形态学正常的新生儿早产
- 在妊娠10周以前发生3次以上的不可解释的自发性流产,必须排除母体解剖、激素异常及双亲染色体异常。
诊断抗磷脂综合征的实验室标准:
- 血浆中出现狼疮抗体,至少发现两次,每次间隔至少12周;
- 用标准的ELISA在血清中检测到中高低度的IgG/IgM类抗磷脂抗体(IgG型抗心磷脂抗体> 40GPL,IgM型康馨磷脂抗体>
40MPL,或滴度> 99百分位数。);至少两次间隔至少12周; - 用标准的ELISA在血清中检测到IgG/IgM型抗β2-GP1抗体至少2次,间隔至少12周( 滴度> 99百分位数)。
诊断抗磷脂综合征必须具备至少一项临床标准和一项实验室标准

抗磷脂综合征的发病机制主要包括由抗磷脂抗体与内皮细胞、滋养层细胞、自然杀伤细胞等靶细胞上的自身抗原相互结合,进而产生炎症相关因子,激活补体后的级联反应为核心的机体免疫活动和损伤。
这些免疫活动和损伤可导致血栓形成,滋养层细胞破坏的最终将导致产科相关不良事件发生。
患者约70%为女性,好发于育龄期。
根据发病原因抗磷脂综合征可分为原发性和继发性。
继发性抗磷脂综合征可继发于系统性红斑狼疮或其他系统性自身免疫性疾病,有30%-80%的系统性红斑狼疮患者合并抗磷脂综合征,其发生严重产科并发症和不良妊娠结局的风险大于单独的系统性红斑狼疮或抗磷脂综合征。
与妊娠相关的抗磷脂抗体,主要类型是狼疮抗凝物、抗心磷脂抗体和抗β 2-GP1抗体,其中狼疮抗凝物阳性者妊娠不良事件的发生率最高。妊娠合并抗磷脂综合征发生并发症的发病率约为30%。
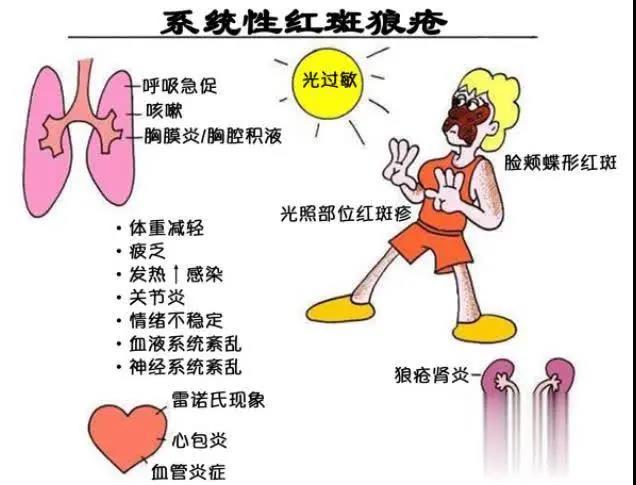
系统性红斑狼疮
系统性红斑狼疮是一种多因素参与自身免疫介导的弥漫性结缔组织病。遗传因素、性激素和环境因素相互作用,引起自身免疫调节功能紊乱,突出表现为B细胞功能亢进,产生多种自身抗体,导致多个系统和器官受累血管病变是其基本病理变化之一,妊娠期常累及胎盘血管。
系统性红斑狼疮孕妇和胎儿发生严重并发症的风险明显高于正常人群。30%-80%系统性红斑狼疮患者血清中存在抗磷脂抗体,这些患者发生严重产科并发症和不良妊娠结局风险更大,其中复发性流产是系统性红斑狼疮最常见的妊娠并发症之一。
复发性流产合并系统性红斑狼疮患者如何备孕?
对于复发性流产合并系统性红斑狼疮的患者,如能耐受,建议患者于计划妊娠前三到六个月开始每天服用羟氯喹(商品名为赛能或美卓乐)0.2-0.4克,可分两次口服,并在妊娠期持续服用羟氯喹至少至产后3个月。
复发性流产合并系统性红斑狼疮未使用糖皮质激素的患者,若无法耐受单纯服用羟氯喹或单纯服用羟氯喹时,出现狼疮疾病活动者,可考虑加用小剂量糖皮质激素(泼尼松≤10mg/d,或等效的其他不含氟的糖皮质激素,如泼尼松龙甲基泼尼松龙等)治疗。
复发性流产合并系统性红斑狼疮的患者,若使用羟氯喹及小剂量泼尼松治疗仍无法控制狼疮活动时,可考虑使用硫唑嘌呤【1.5-2mg/(kg•d),分两次服用】、环孢素【3-5 mg/(kg•d),分两次服用】或他克莫司(2-3mg/d,每12小时服用一次)等妊娠期相对安全的免疫抑制剂。
复发性流产合并系统性红斑狼疮的患者,妊娠期若狼疮出现中、重度活动或狼疮肾炎患者出现顽固性肾病综合征,可考虑静脉使用糖皮质激素[如甲基泼尼松龙0.5-1mg/(kg•d)静脉滴注]静注人血免疫球蛋白400mg(kg•d),连续输注3-5天]和/或血浆置置换等治疗。
复发性流产合并系统性红斑狼疮的患者在多药治疗无效、狼疮活动严重的患者中,可于妊娠中、晚期使用环磷酰胺(500-1000mg/㎡,每月一次静脉滴注),并考虑终止妊娠。

未分化结缔组织病
患者出现一种或一种以上结缔组织病的症状或体征,以及一种或一种以上的自身抗体(如抗核抗体、抗SSA抗体等)阳性,病程持续一年以上,但又不符合任何结缔组织病诊断标准的自身免疫病,可能是自身免疫异常到结缔组织病的一种过渡状态。研究显示,未分化结缔组织病对妊娠和胎儿的影响明确,可导致流产/死产、子痫、胎儿生长受限、新生儿先天性心脏传导阻滞、新生儿狼疮等。同时,会增加部分为分化结缔组织病的患者发展为结缔组织病的风险。
以育龄期女性多见,性别与发病有关,男女比例为1:6-1:4,患者体内存在的自身抗体或细胞因子在妊娠期会影响胎盘功能,增加不良妊娠结局的发生率,同时,妊娠会增加未分化结缔组织病转化为系统性红斑狼疮、抗磷脂综合征、硬皮病、炎症性肌病、干燥综合征等疾病的风险。
在妊娠过程中可能出现严重并发症,如血小板进行性减少或血栓性血小板减少性紫癫、心肌炎、非特异性间质性肺病、心血管疾病、血管炎、心包填塞、肝损害等。因此,要重视复发性流产人群中未分化结缔组织病的筛查和诊断。复发性流产合并未分化结缔组织病妊娠期常用的免疫抑制机有:羟氯喹、糖皮质激素、环孢素、他克莫司、硫唑嘌呤、免疫球蛋白等。
目前的研究认为未分化结缔组织病的发生与母胎免疫耐受失衡有关,被认为是一种同种免疫病,但其发病机制尚不完全清楚,由于病因及发病机制不明,对未分化结缔组织病的治疗目前仍缺乏公认的有效的治疗手段,尚无足够的证据表明免疫治疗有效,比如丈夫或无关个体的淋巴细胞主动免疫治疗和免疫球蛋白、环孢素、糖皮质激素以及羟氯喹的治疗方法,虽然需要更多的研究来证实上述方法的有效性,或探索其他治疗方法。
由于未分化结缔组织病的发病机制尚不清楚、目前仍缺乏公认的有效的治疗手段,因此在临床上不推荐使用免疫抑制剂、免疫调节剂,如糖皮质激素、羟氯喹、免疫球蛋白、环孢素、淋巴细胞主动免疫治疗等方法作为未分化结缔组织病的常规治疗方案,除非在综合分析病情后并充分取得患者知情同意的情况下,酌情进行临床实验性用药。
干燥综合征
干燥综合征是一种以唾液腺、泪腺等外分泌腺体受累的慢性炎症为主要特征,并可累积全身多系统的自身免疫性疾病。在遗传、感染、性激素等多种因素作用下,机体免疫功能紊乱,可出现大量淋巴细胞、浆细胞及单核细胞在肌底层侵润,同时伴有导管上皮细胞增生形成病灶的病理改变。干燥综合征患者妊娠时,胎盘可作为靶器官而受到免疫损害,造成胎盘功能障碍,从而增加妊娠并发症和胎儿丢失发生的风险,干燥综合症患者和正常人群相比,自然流产率和早产率明显增加。
可根据表现不同分为原发性和继发性两类,约各占50%,抗SSA(Ro)和SSB(La)抗体是诊断干燥综合征较为特异的抗体。干燥综合征患者中80%抗SSA抗体阳性,50%抗SSB抗体阳性,抗S S A抗体是影响胎儿预后的标志物。
研究表明,如干燥综合征同时合并系统性红斑狼疮时自然流产率和早产率都显著增加,抗SSA和(或)抗SSB抗体阳性患者,妊娠期易导致胎儿和新生儿先天性心脏传导阻滞,甚至引发胎儿心脏骤停,其发生率为2%,且再次妊娠胎儿心脏骤停的风险明显增加。患儿死亡率为30%。即使能存活,67%的患儿需安装心脏起搏器。
干燥综合征的患者同时合并抗磷脂抗体则流产、早产、溶血、肝酶升高、血小板减少、子痫和胎盘血肿的发病风险增加,研究显示,在抗SSA/Ro抗体阳性的干燥综合征患者中,使用羟氯喹可减少胎儿先天性心脏传导阻滞的发病风险。