Eprenetapopt联合阿扎胞苷可改善伴TP53突变MDS患者的疗效
伴TP53突变的骨髓增生异常综合(MDS)和急性髓系白血病(AML)患者预后差、生存期短,缺乏有效治疗手段。有研究者开展了一项Ib/II期临床研究,旨在评估Eprenetapopt(APR-246)联合阿扎胞苷在伴TP53突变的MDS或AML(骨髓原始细胞比例20%~30%)患者中的安全性及疗效,近日其相关结果公布在《临床肿瘤学杂志》(Journal of Clinical Oncology)上。
研究背景
初诊MDS和AML患者中TP53基于突变率约10%~20%;而治疗相关的MDS和AML患者中TP53基因突变率约30%~40%。伴有TP53基因突变的MDS和AML患者缺乏有效治疗手段、预后差、生存期短。去甲基化药物(HMA)在TP53突变或野生型MDS患者中完全缓解(CR)率相似、约为15%~20%。然而,伴TP53突变的患者缓解期短、中位总生存期(OS)为5~12个月,针对伴TP53突变的MDS和AML患者未满足的临床需求仍很大。
Eprenetapopt(APR-246)是一种新型、小分子药物,可选择性诱导TP53突变的癌细胞发生凋亡。临床前研究结果显示Eprenetapopt与阿扎胞苷联合作用于TP53突变的MDS和AML细胞系(包括患者标本和体内模型),具有协同的细胞毒性作用。研究者们开展一项Ib / II期临床研究,旨在评估Eprenetapopt联合阿扎胞苷治疗TP53突变的髓系恶性肿瘤(以MDS和AML为主)患者的安全性和疗效。
研究方法
该研究是一项开放标签、多中心剂量递增和剂量扩展的Ib / II期临床研究。初始剂量递增阶段采用标准的3+3设计评估了Eprenetapopt与阿扎胞苷联合的剂量限制毒性(DLT),以建立推荐的II期剂量(RP2D)。Eprenetapopt在每个治疗周期的第1-4天以静脉输注形式给药,阿扎胞苷的标准剂量为75 mg/m2(连续7天,第4-10天或2 + 5天(即第4-5天和8-12天)皮下注射或静脉输注给药,28天为1个治疗周期。由于在Ib期研究中未发生DLT,因此在II期中Eprenetapopt为4500 mg/患者/天的固定剂量(根据人群药代动力学模型,等效剂量为100 mg/kg/d LBM)。
该研究纳入的患者为≥18岁、ECOG评分为0-2分、肝肾功能良好,既往未使用过HMA的MDS、MDS/骨髓增生性肿瘤(MDS/ MPN)、慢性粒细胞性白血病(CML)或AML(原始细胞比例20%~30%)的患者;且所有患者均使用二代测序(NGS)检测明确具有TP53突变。
II期研究的主要终点是完全缓解(CR)率;次要终点为总有效率(ORR)、治疗反应持续时间(DOR)和OS。此外,该研究还通过高灵敏度NGS分析了TP53突变克隆的微小残留病(MRD)状态。
研究结果
该研究患者入组时间为2017年5月至2019年2月,数据截止时间为2019年11月15日,此时所有患者入组≥6个月。共有55例(40例为MDS、11例为AML、4例为MDS/MPN)符合条件的患者接受了Eprenetapopt联合阿扎胞苷治疗,其中12例处于剂量递增阶段(包括6例接受RP2D治疗的患者)和43例处于II期剂量增加阶段。患者的基线人口统计学和临床特征(详见表1);各个患者分子和细胞遗传学特征的热图(详见图1)。患者的中位年龄为66,女性为53%;MDS患者中93%的患者依据R-IPSS为较高或非常高风险、69%的患者基线时依赖输血。
表1:意向治疗(ITT)人群基线人口学特征和临床特征
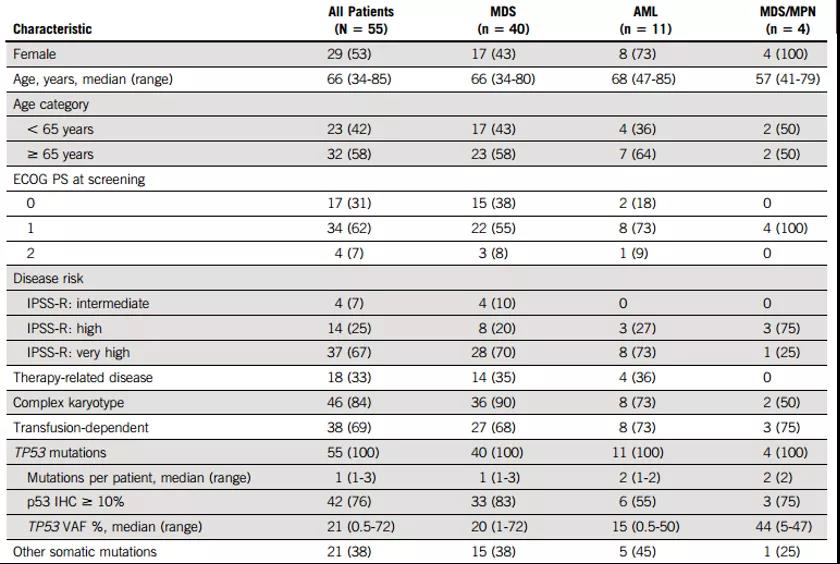
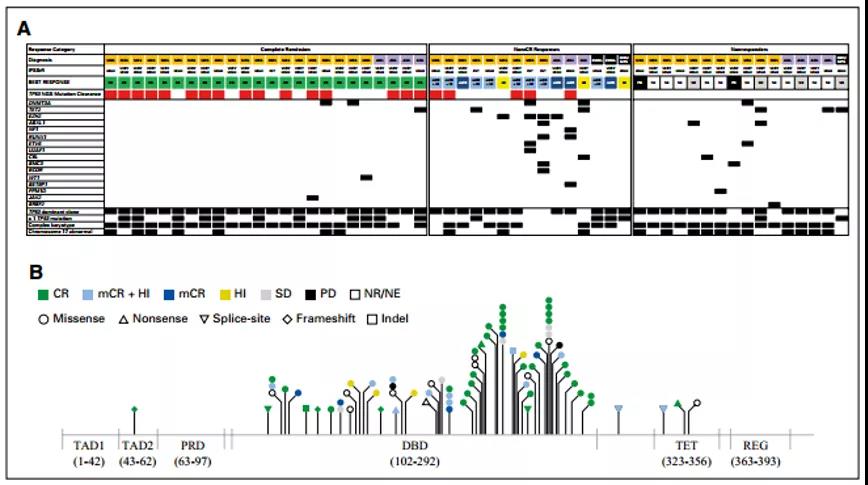
图1:(A)各个患者基线细胞遗传学风险特征的热图 ;(B)最佳响应的TP53突变类型和位置的火柴图
该研究中接受Eprenetapopt和阿扎胞苷联合治疗的患者最常见的≥3级不良事件(AE)是发热性中性粒细胞减少症(33%)、白细胞减少症(29%)、中性粒细胞减少症(29%)、血小板减少症(25%)和肺部感染(25%),其中<5%的≥3级AE被认为可能与Eprenetapopt治疗有关。
意向治疗(ITT)人群中接受联合治疗的患者中, MDS队列的ORR为71%、CR率为50%,AML队列的ORR为64%、CR率为36%。在39例有治疗反应的患者中,有35例(90%)患者按照国际工作组标准具有血液学改善。
该研究中治疗反应可评估的患者共45例。整体队列的ORR为87%:MDS(n =29)和AML(n = 7)队列的ORR均为88%。整体队列的CR率为53%:MDS队列为61%,AML队列为50%。具有细胞遗传学反应的患者占59%(部分反应为18%、完全反应为41%);在MDS队列中反应最高为70%(部分反应为24%,完全反应为46%)。患者ORR和CR的中位持续时间在MDS和AML队列间无显著差异。
中位随访时间为10.5个月时,ITT人群的中位OS为10.8个月(95%CI,8.1~13.4;图2A),MDS患者中位OS为10.4个月(95%CI,7.6~13.3)和AML患者中位OS为10.8个月(95%CI,5.1~16.5)。探索性分析显示,在治疗4个月时治疗有效较无效的患者具有更长的中位OS(14.6个月;95%CI,12.4~16.8)vs(7.5个月;95%CI,6.1-8.7个月;危险比-HR,0.23; P = 0.0005;图2B)。在第4个月时的分析显示,与治疗无效的患者相比,达到CR和非CR反应的患者的OS均显著改善(P = 0.001;图2C), 尽管在治疗有效的患中CR和非CR患者之间的中位OS并无显著差异(12.8个月 [ 95%CI,10.8~14.7] vs 14.7个月 [95%CI,8.4~21.1]; P = 0.63;图2C)。桥接移植患者的中位OS为14.7个月(95%CI,8.6~20.9)。
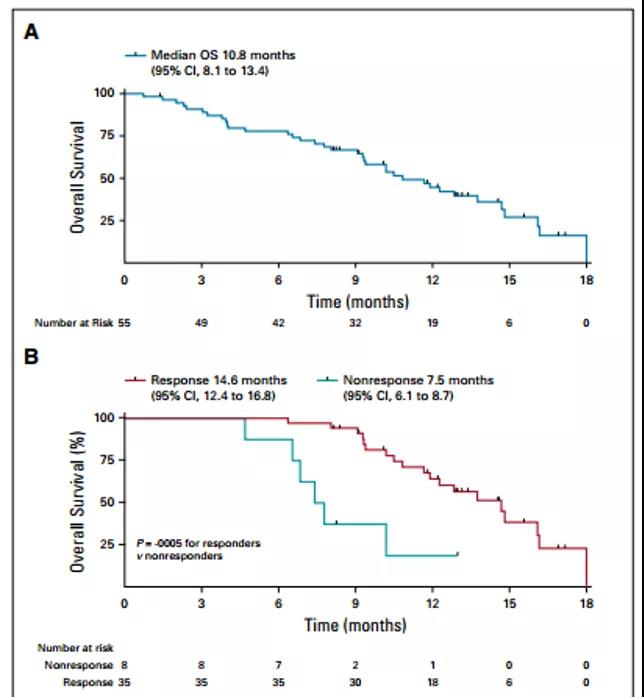
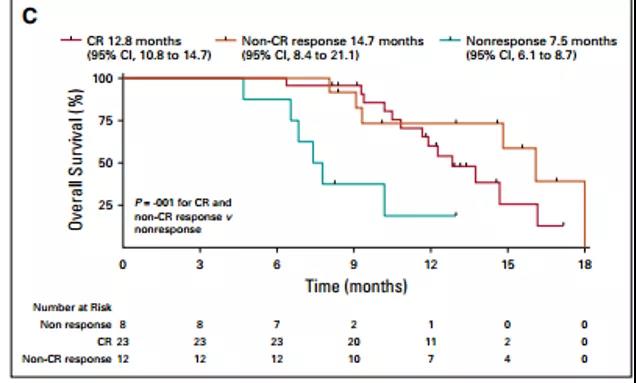
图2:(A)ITT人群的OS情况,(B)治疗有效患者的OS情况,(C)在4个月时治疗无效和治疗疗效(CR及非CR)患者的OS情况
另外,通过NGS检测仅存在TP53突变的患者,与同时存在其他突变的患者相比, CR率明显更高(69% vs 25%; P = 0.006)。基线时免疫组织化学(IHC)检测p53蛋白+的骨髓(BM)单个核细胞≥10%与患者CR率显著相关(66% vs 13%; P = 0.01)。共有21例(38%)患者达到了NGS检测的TP53突变阴性。TP53 VAF清除率与CR显著相关(P <0.0001),且非CR患者的清除率呈上升趋势(P = 0.061)。治疗无效的患者中TP53 VAF清除率无明显变化(P = 0.87)。获得CR患者的TP53 VAF显著低于非CR的患者(P <0.001)。同样,基于IHC检测的p53蛋白清除率与患者CR显著相关(P<0.0001),非CR患者(P=0.066)和治疗无效患者(P=0.052)轻度降低。
研究结论
该研究表明,对于伴TP53突变的MDS和原始细胞比例低的AML患者,使用Eprenetapopt联合阿扎胞苷治疗具有良好的耐受性,且具有较高的CR率和细胞遗传学应答率。
参考文献
David A Sallman,Amy E DeZern,Guillermo Garcia-Manero,et al.Eprenetapopt(APR-246)and Azacitidine in TP53-Mutant Myelodysplastic Syndromes. J Clin Oncol.2021 Jan 15;JCO2002341.