液体活检获得的 CTC 的转录谱结果可作为转移性前列腺癌患者的孤立预后标志物并预测耐药
几乎所有接受雄激素受体(AR)信号抑制剂(ARSI)治疗的前列腺癌男性都会通过多种机制产生耐药性,包括 AR 通路的激活,AR 基因结构改变、AR 剪接变体(AR-V)的表达或 AR 依赖性和谱系可塑性的丧失。了解这些 de novo 获得的 ARSI 耐药机制对于优化治疗至关重要。
材料和方法:一种新型液体活检技术用于从循环肿瘤细胞(CTC)中收集 mRNA,以测量 AR-V、AR 靶标和神经内分泌前列腺癌标志物的表达。机构审查委员会批准的前瞻性队列(N = 99)用于确定基因表达模式。两项针对去势抵抗性前列腺癌男性 ARSI 的前瞻性多中心 II 期临床试验(ClinicalTrials.gov:NCT01942837 [enzalutamide,N = 21] 和 NCT02025010 [abiraterone,N = 27])被用于进一步验证这些发现。
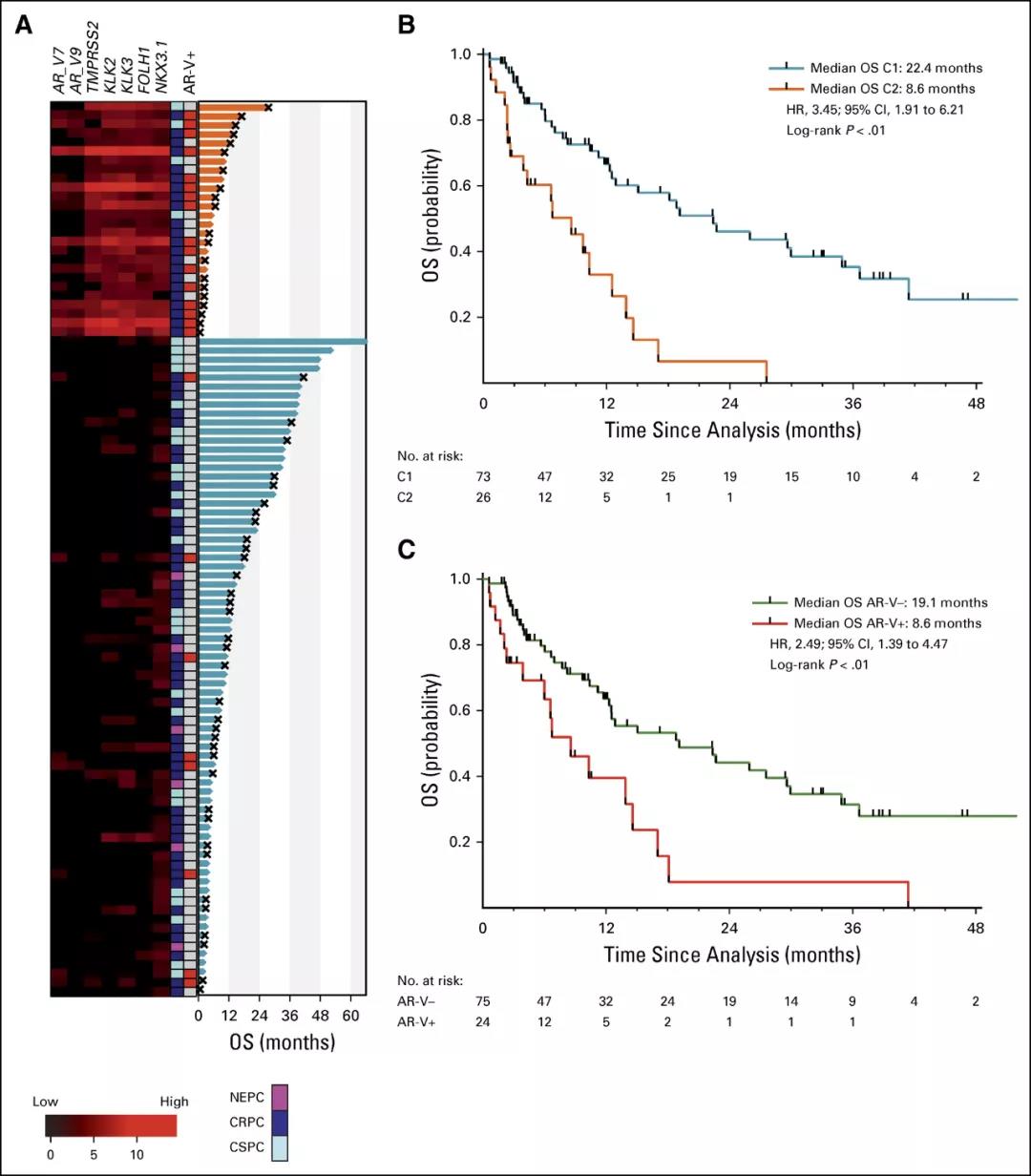
结果:CTC 转录本的分层聚类确定了两个不同的聚类。聚类 2(C2)表现出 AR 调节基因的表达增加,并与较差的总生存期相关(中位 8.6 个月 vs 22.4 个月;P< 0.01;HR = 3.45 [95%CI:1.9 - 6.14])。
(图源:参考文献)
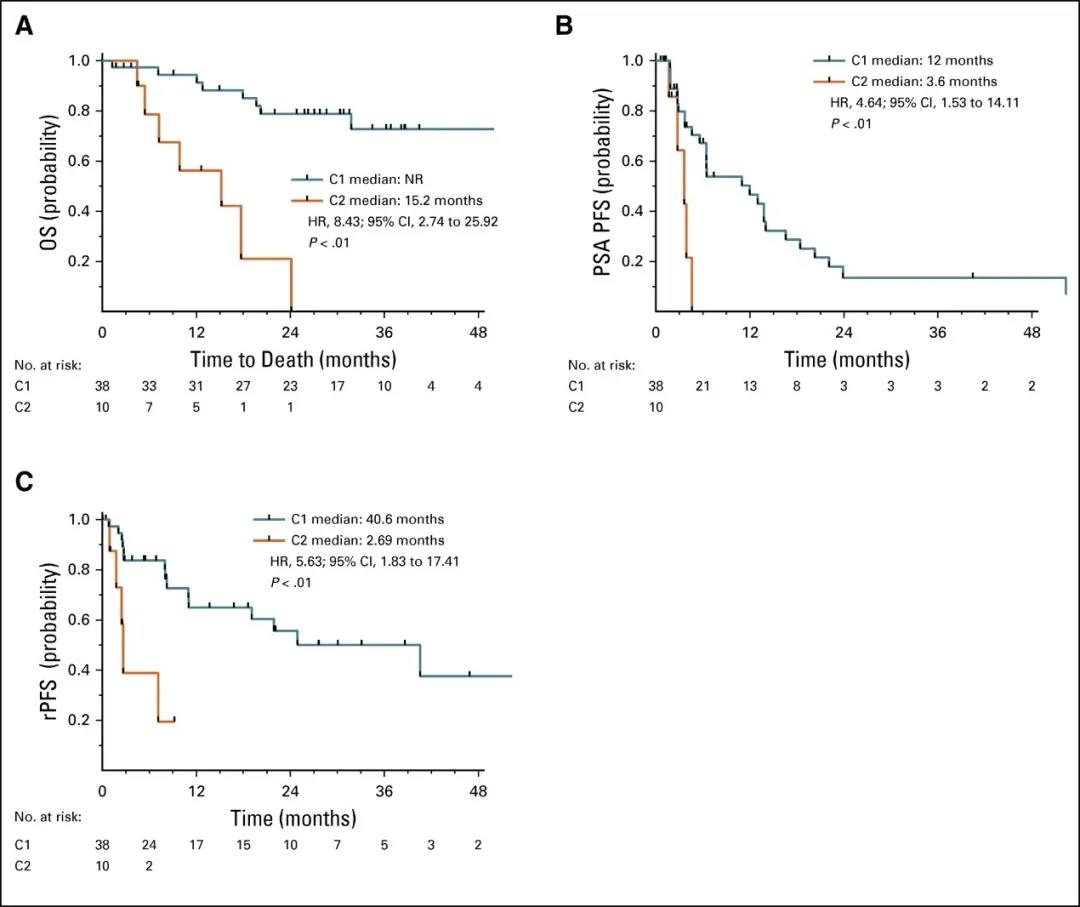
在多变量分析中,C2 是孤立于其他临床病理变量的预后。在考虑 C2 时,AR-V 状态并不显著。在汇总的多中心 II 期试验中进一步验证后,C2 与较差的总生存期(15.2 个月 vs 未达到;P< 0.01;HR = 8.43 [95%CI:2.74 - 25.92])、前列腺特异性抗原无进展生存期(3.6 个月 vs 12 个月;P<0.01; HR = 4.64 [95%CI:1.53 - 14.11]),影像学无进展生存期(2.7 个月 vs 40.6 个月;P< 0.01;HR = 4.64 [95%CI:1.82 - 17.41])。
(图源:参考文献)
结论:我们证明,从液体活检获得的 CTC 中可检测到的转录谱可以作为 AR-V7 以外的转移性前列腺癌患者的孤立预后标志物,并可用于识别多种 ARSI 耐药机制的出现。目前正在其他前瞻性试验中对此进行进一步研究。