程颖教授 SCLC免疫治疗有喜有悲,未来可期
如同今年的中秋和国庆,两大顶级肿瘤学术会议2020 ESMO和2020 CSCO也在同一时间召开。一时间,各领域的研究结果集中爆发,引发了全球学术热潮。CCMTV特邀吉林省肿瘤医院程颖教授,就SCLC免疫治疗的现状及ESMO上STIMULI研究的相关结果进行解读。

程颖教授:免疫治疗改变了小细胞肺癌的治疗格局,为小细胞肺癌一线治疗带来了新的标准,也为三线及以上SCLC的治疗建立了标准治疗选择。
根据Impower133研究和caspian研究atezo联合卡铂/依托泊苷,durval联合卡铂或者顺铂/依托泊苷成为广泛期小细胞肺癌新的一线治疗选择,从更新的数据中依然看到OS的获益,进一步巩固了atezo联合化疗和durval联合化疗作为ES-SCLC一线治疗的新标准。
而caspian 研究durval+tremelimumab+化疗4药治疗组的数据中看到,与化疗相比,4药治疗并没有带来OS和PFS的获益,反而增加了毒性。除了PD-L1抑制剂外,PD-1抑制剂联合化疗一线治疗广泛期小细胞肺癌也有数据公布。KEYNOTE604研究是一项pembro联合化疗一线治疗广泛期小细胞肺癌的3期随机对照研究,研究发现与化疗相比,pembro联合化疗能够获得PFS的改善,但OS没有获得统计学意义的改善,nivo联合化疗一线治疗广泛期小细胞肺癌的2期研究同样也只有PFS的改善没有OS的显著改善。
目前这些研究出现不同的结果考虑与研究选择的人群、研究设计、药物差异、后续治疗等因素有关,提示免疫治疗在小细胞肺癌还需要更多的探索,包括标志物的选择和治疗模式的探索。

除了在小细胞肺癌一线治疗领域,免疫治疗在复发SCLC也有新的结果公布。TQB2450(PD-L1抑制剂)联合安罗替尼治疗晚期实体瘤的单臂、开放、Ib期剂量探索研究中纳入了6例SCLC患者,4例获得PR的疗效。而一项免疫联合抗血管药物二线治疗小细胞肺癌的2期研究中看到卡瑞利珠单抗联合阿帕替尼二线治疗广泛期SCLC的ORR达33.9%,中位的OS为8.4个月,即使是在耐药的患者中位的OS也达到了8.0个月,提示免疫联合抗血管治疗是复发小细胞肺癌充满前景的治疗策略。
看见免疫联合抗血管治疗在SCLC充满前景,目前在化疗的基础上免疫联合抗血管一线治疗广泛期SCLC的正在如火如荼的进行中,期望能够为广泛期小细胞肺癌带来更大的获益。

程颖教授:放化疗作为局限期小细胞肺癌的标准治疗模式已经30余年未曾改变了。随着免疫治疗在复发SCLC和广泛期小细胞肺癌一线治疗取得突破,研究者也把改善局限期小细胞肺癌治疗现状的希望寄于免疫治疗。
广泛期SCLC诱导化疗后pembro联合胸部放疗的一项1期研究中pembro与胸部放疗联合具有良好的耐受性,短期内严重毒性少见,免疫联合放疗的安全性为进一步在局限期SCLC开展放化疗联合免疫治疗研究提供依据。

目前在局限期SCLC中开展的免疫联合放化疗的研究主要聚焦在放化疗后的巩固免疫治疗以及放化疗同步免疫治疗,ADRIATIC研究是一项局限期SCLC放化疗后巩固治疗的国际多中心的3期研究,这项研究正在招募入组中。另外罗氏将在中国开展一项2期的局限期SCLC同步或者续贯放化疗中开始进行阿替利珠单抗免疫治疗的研究,此外国产的免疫检查点抑制剂在局限期SCLC的免疫治疗也将开启,这些研究将为我们阐释局限期SCLC的免疫治疗如何进行更有效,更安全,这些研究可能成为未来改变局限期SCLC治疗格局的基础。

程颖教授:自免疫治疗改变ES-SCLC和复发SCLC的治疗格局以来,也一直期待免疫治疗能够迎来局限期SCLC治疗策略的变革。一项Pembro 联合同步放化疗治疗局限期SCLC或其他肺神经内分泌肿瘤的单臂单中心I/II期研究中纳入40例患者入组,其中36例SCLC,33例可评估,ORR为79%,SCLC中位的PFS为22.2个月,OS尚未达到。
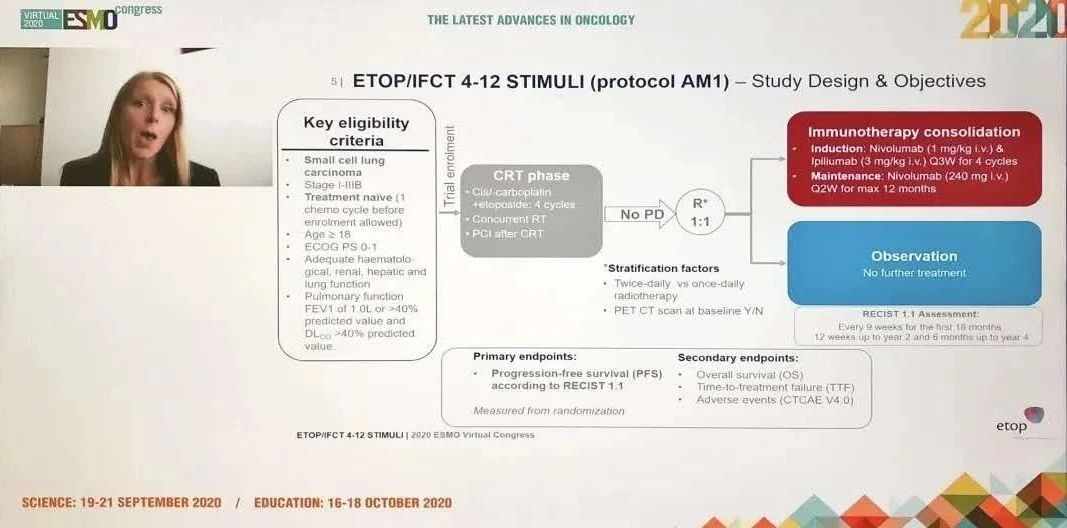
在今年ESMO上,也刚刚公布了一项局限期SCLC放化疗后伊匹木单抗+纳武利尤单抗巩固治疗与等待观察进行对照的随机2期研究,这项研究纳入完成同步放化疗和PCI后没有进展的局限期SCLC,比较伊匹木单抗+纳武利尤单抗4周期后纳武利尤单抗维持最长12个月或者观察治疗,经过中位22.7个月的随访,发现伊匹木单抗+纳武利尤单抗巩固治疗局限期SCLC并没有获得PFS的显著获益,但是在PFS亚组分析中接受每日2次放疗的患者PFS有获益趋势,这与既往局限期小细胞肺癌的研究中每日2次放疗的患者获益更多结果一致。虽然ECOG 评分1分和女性患者PFS有获益的趋势,但研究并没有按照这两个因素进行分层,结合亚组样本量的差异,需要谨慎解释。
目前这项研究巩固治疗组的OS还没有达到,尽管两组OS尚未发现有统计学差异,但从OS曲线看到两组在30个月后免疫巩固治疗组的OS曲线逐渐超过观察组,免疫治疗组36个月的OS率超过观察组近13%,看到免疫治疗持久的获益。从安全性看,≥3级AE明显多于观察组,免疫巩固治疗组有大约一半的病人因治疗相关毒性导致治疗终止,数据截止时免疫巩固治疗组65例治疗失败的患者中36例是由于毒性,15例是由于疾病进展,而观察组中44例治疗失败的患者中,有35例是因疾病进展。可能由于双免疫巩固治疗通过毒性效应导致患者接受巩固治疗的患者受限,导致两组没有获得PFS的差异。