免疫化疗联合来那度胺,一线治疗MCL效果如何?用PET-CT和MRD结果说话!
摘要
目前套细胞淋巴瘤(MCL)一线强化疗方案联合自体造血干细胞移植虽然可以显著延长患者复发时间,但如何提高一线治疗疗效仍是临床医生和研究人员不断探索的目标与方向。2020年,在第62届美国血液学会年会(ASH 2020)上,一项探索MCL一线治疗方案的重磅研究为MCL患者带来了新的希望。
套细胞淋巴瘤一线治疗变革
MCL是一种侵袭性B细胞淋巴瘤,对于适宜的患者通常采取免疫化疗联合高剂量巩固治疗+干细胞挽救(cHDT/SCR)治疗,然而在一项随机试验中,该治疗方法尚未证实总生存(OS)获益。经干细胞挽救(cHDT/SCR)治疗后,高风险MCL患者(TP53异常、高增殖指数、组织学呈原始状态)的预后仍较差,因此,并非所有的MCL患者都适宜该方法。
鉴于此,在ASH 2020大会上,美国纪念斯隆凯特琳癌症中心的Zachary D,Epstein-peterson教授报道了其所在团队主导的一项II期临床研究数据,表明在序贯免疫化疗联合来那度胺治疗MCL的新疗法中,TP53突变患者的预后较差,未达到3年无疾病进展生存期(PFS)≥75%的主要研究终点。而在野生型TP53的患者中,即使对于Ki67≥30%的患者,该治疗方案仍非常有效,缓解率较高,3年PFS率可达85%,治疗结束时微小残留病(MRD)阴性比例较高。

三阶段治疗,构成MCL新型一线治疗方案
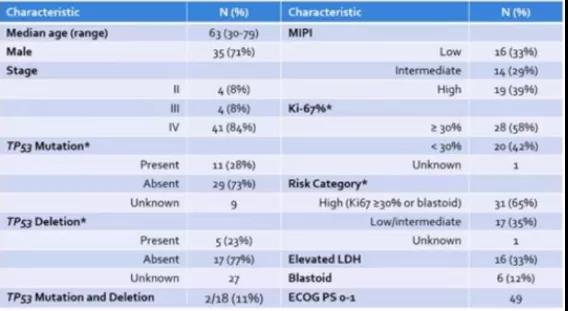
该研究(摘要119)旨在探索在MCL患者,包括高危患者(定义为胚样/多形组织学和/或Ki67≥30%)接受序贯免疫化疗联合来那度胺治疗情况。
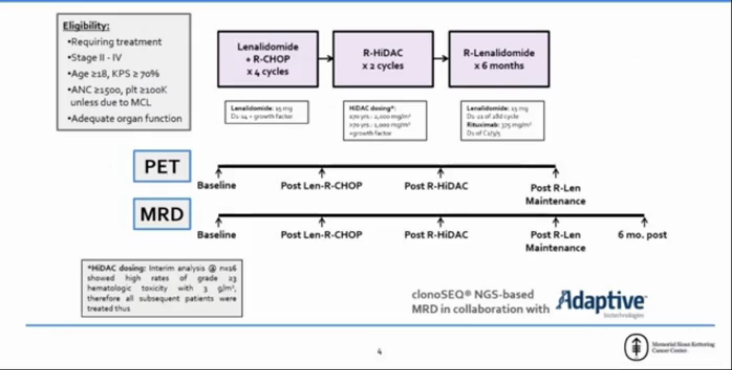
治疗过程分为三个阶段:
来那度胺(每天15mg,第1-14天)+R-CHOP,21天为一周期,共4个周期;
R-HiDAC共2个周期(基于年龄阿糖胞苷起始量为1-3g/m2;16例患者发生血液学毒性后取消3g/m2的剂量);
每月使用1次利妥昔单抗+来那度胺(每天15mg),共治疗6个月。
使用clonoSEQ分析法对外周血(细胞DNA)进行MRD评估;每个治疗阶段完成后均进行PET/CT和MRD评估,并在利妥昔单抗+来那度胺维持治疗6个月后进行MRD评估。主要研究终点是3年无进展生存(PFS)率(根据高危患者的预期比例,PFS≥75%可接受,PFS≤60%不可接受)。
总缓解率高达91%,全部达到CR!
在纳入研究的49例患者中,47例可评估PFS[来那度胺-R-CHOP治疗期间1例患者疾病进展(PD),1例患者出现治疗毒性],45例患者完成了维持治疗(1例在R-HiDAC期间PD,1例退出研究进行了cHDT/SCR治疗),43例患者达到完全缓解(CR),1例患者疾病稳定(SD),1例在治疗结束时PD。
总缓解率(ORR)为91%,均为CR。
生存患者的中位随访时间为2.8年,3年PFS率为64%(95%CI:50-82),OS率为85%(95%CI:74-99)。
不同TP53状态的3年PFS率不同(突变型14%vs野生型85%,P<0.0001)。在4例PD患者中,3例伴有TP53突变,1例突变类型未知。在野生型TP53患者中,按风险分层的预后无显著差异。
45例患者获得了MRD结果,其中87%(39/45)的患者成功完成了用于MRD评估的肿瘤克隆鉴定。
在来那度胺-R-CHOP治疗后的37例患者中,以1x10-5(1E5)的灵敏度检测初始治疗(来那度胺-R-CHOP和R-HiDAC)的MRD结果,仍有相当比例(32%,12/37)的患者为MRD+,其中11例来那度胺-R-CHOP治疗后MRD+的患者经R-HiDAC治疗后转为MRD-。以1x10-6灵敏度(1E6)检测经R-HiDAC治疗的患者,其中5/20例患者为MRD+。在有缓解的患者中,MRD+相对于MRD-患者中位PFS较短(23.1个月vs NR,P=0.03)。
治疗的最后阶段(利妥昔单抗+来那度胺维持)和观察期,治疗结束时37例患者有1E5 MRD结果,4例为MRD+,其中2例(在评估2周内)复发,其余2例MRD+患者的中位PFS为4.9个月,而32例无复发MRD-患者的中位PFS为37.4个月(P<0.001)。经过6个月的观察,治疗结束时处于MRD-的6例患者转为MRD+(1E6)。
治疗结束后6个月1E6 MRD状态与PFS相关:在20例无复发患者中(6例MRD+,14例MRD-),MRD-患者的中位PFS为30.8个月,而MRD+患者的中位PFS为13.2个月(P=0.02)。
研究结论
随着研究的不断深入,发现沙利度胺在MCL患者治疗中的应用可去的一定的价值,沙利度胺可发挥免疫调节以及抗血管新生的作用,抗肿瘤效果好。
在本研究中,序贯免疫化疗联合来那度胺用于治疗MCL(包括65%的高危患者),其中,TP53突变患者的预后较差,并且未达到3年PFS率≥75%的主要研究终点。在野生型TP53患者中,即使对于Ki-67升高(≥30%)的患者,该治疗方案也非常有效,缓解率较高,3年PFS率可达85%,治疗结束时MRD-比例较高。
很多患者在R-HiDAC治疗后转为MRD-,这突出了阿糖胞苷在MCL中的疗效。诱导化学免疫治疗(来那度胺-R-CHOP+R-HiDAC)后,1E5(97%)和1E6(80%)MRD-率较高,且后者可预测缓解持续时间。在治疗结束6个月后,数例患者从MRD-转为MRD+并最终复发,这表明更长时间的维持治疗可能是有益的。另外,患者在治疗结束后6个月的1E6 MRD可预测缓解持续时间。
张会来教授点评:
这项序贯免疫化疗联合来那度胺治疗MCL的研究口头报道,的确是一个不同于以往治疗模式的探索。我个人认为该研究的研究设计与美国MD安德森肿瘤中心王鲁华教授领衔的window-1研究有些相似。从干预措施上来看,此项研究是序贯免疫化疗联合来那度胺,而window-1研究则是伊布替尼以及利妥昔单抗(IR)联合短疗程R-Hyper CVAD/MTX方案一线治疗MCL,比较不同的一点是该研究还设计了维持治疗阶段。
该研究在治疗的第一阶段采取了来那度胺+R-CHOP联合治疗,21天为一周期,共4个疗程;第二阶段采取了两个周期的大剂量阿糖胞苷治疗;第三阶段则采取利妥昔单抗+来那度胺的六个月维持治疗。但同时我们也要考虑来那度胺长期应用之后以及完成这样三阶段的治疗后是否会影响患者的干细胞收集。
另外该研究也存在一定的优势——PET-CT与MRD联合用于疗效预后评估更加合理也准确。这样相结合的评估方式在未来也会更加有临床应用价值。
从研究结果上来看,非常值得一提的是在TP53野生型的患者中,即使对于Ki67≥30%的患者,该治疗方案非常有效,缓解率较高,3年PFS率可达85%,治疗结束时MRD-比例较高。同时基于TP53状态的亚组分析提示:不同TP53状态的3年PFS率显著不同(突变型14%vs野生型85%,P<0.0001)。在4例PD患者中,3例伴有TP53突变,1例突变类型未知。在野生型TP53患者中,按风险分层的预后无显著差异。
并且该研究再次证实了阿糖胞苷在MCL治疗中的地位和价值,确实可以助力患者MRD转阴。但试验中第三阶段六个月维持治疗结束之后,仍有部分患者MRD转阳,最终复发。这也提示了临床医生:六个月的维持治疗可能还不足够,或许需要更长的治疗周期或是选择新药物纳入维持治疗。
专家简介

张会来 教授
肿瘤学博士,主任医师,博士研究生导师
现任天津医科大学肿瘤医院淋巴瘤内科主任
主要研究方向:恶性淋巴瘤的分子诊断和个体化治疗
中国抗癌协会淋巴瘤专业委员会副主任委员
中国临床肿瘤学会(CSCO)抗淋巴瘤联盟常委
中国医疗保健国际交流促进会肿瘤内科分会副主任委员
中国老年保健协会淋巴瘤专业委员会副主任委员
中国临床肿瘤学会(CSCO)肿瘤心脏病学专委会常委
中华医学会肿瘤分会淋巴瘤学组委员
中国抗癌协会整合肿瘤心脏病学专委会委员
天津市抗癌协会淋巴瘤专业委员会主任委员
天津市血液病质控中心副主任委员
天津市医师协会血液医师分会副会长
曾获天津市科技进步二等奖1项及三等奖3项
主持及参与多项国家自然科学基金课题及省部级科研项目
《中华血液学杂志》、Hematological Oncology、Blood Research等国内外期刊杂志编委
以第一或通讯作者在Blood、International Journal of Cancer、Leukemia&Lymphoma、Medical Oncology、Oncotarget等国际专业杂志以及中华系列杂志、国家级核心期刊发表论著四十余篇
从事肿瘤内科临床工作23年,专注于恶性淋巴瘤分子诊断和个体化治疗研究