探索维奈克拉耐药机制之后,CLL患者治疗该如何继续?
慢性淋巴细胞白血病(CLL)包括具有传统高危因素如del(17p)或复杂染色体核型种种类型,经BCL2抑制剂Venetoclax(维奈克拉)治疗后可获得深而持久的治疗反应。
基于CLL14和MURANO研究的结果,维奈克拉联合抗CD20单克隆抗体目前已成为初诊CLL和复发或难治性CLL(R/R CLL)患者的标准治疗。由于该方案在临床实践中使用频率的增高,预期会有越来越多的CLL患者在前期治疗中使用基于维奈克拉治疗方案,但其在复发或进展后仍面临对后续治疗方案进行选择。本文主要讨论维奈克拉耐药的机制,并为耐药患者选择合适的后续治疗方案提供建议。
维奈克拉耐药机制
笔记1:
CLL患者停用维奈克拉最常见的原因是出现疾病进展(PD)而非治疗相关的不良事件(AE)。
既往是否使用过BTK抑制剂(BTKi)、前期治疗线数、是否伴高危细胞遗传学突变以及微小残留病(MRD)状态等是预测CLL患者使用基于维奈克拉方案治疗后是否出现疾病进展(PD)的相关因素。
一项回顾性研究纳入445例R/R CLL患者,结果显示既往使用过BTKi、前期治疗线数≥3线以及巨大淋巴结,伴del(17p)、TP53突变、NOTCH1突变以及IGHV未突变是患者接受维奈克拉治疗缓解持续时间短的相关因素。
一项包含67例R/R CLL患者的研究结果显示,复杂核型和氟达拉滨(Flu)难治是其使用维奈克拉治疗后PD的相关因素。
MURANO研究中位随访36个月时的数据显示,对于完成维奈克拉联合利妥昔单抗24个月治疗的CLL患者,治疗结束时MRD仍可测较MRD不可测(uMRD)的患者发生PD的几率更大。此外,在治疗结束时仅达到部分缓解(PR)且MRD可测的患者与uMRD患者相比,治疗后18个月时的无进展生存期(PFS)较差。
笔记2:
通过检测CLL患者是否存在BCL2 Gly101Val突变,或可提前识别使用维奈克拉治疗后出现PD的人群;
克隆演化的异质性和基因组的不稳定性等均与维奈克拉耐药相关。
前临床研究显示特定位点的突变可以竞争BCL2的位点,可能是维奈克拉耐药的机制之一,BCL2 Gly101Val突变的存在使得BCL2对维奈克拉的亲和力降低了约180倍。
一项纳入了15例CLL患者,并对使用维奈克拉治疗后出现早期进展患者样本进行检测,结果显示有7例患者存在BCL2 Gly101Val突变。
另一项研究检测了接受维奈克拉和利妥昔单抗治疗1年后MRD仍持续可测患者的CLL细胞,在6例MRD持续可测和疾病进展的患者中,有3例(50%)出现了BCL2 Gly101Val突变。
近年一项研究将CLL患者接受维奈克拉治疗前和治疗出现进展期间采集的8个样本进行了全基因组测序,并没有检测到BCL2 Gly101Val突变,但研究人员在这些患者疾病发展过程中发现了越来越多的获得性拷贝数突变。这也提示维奈克拉治疗会导致CLL患者出现克隆演化的异质性,且增加基因组不稳定性。
维奈克拉治疗后进展或复发CLL患者的后续治疗选择
笔记3:
一线使用基于维奈克拉的治疗方案,治疗有效但在完成治疗后出现PD或复发且无获得性耐药突变(BCL2 Gly101Val)的CLL患者,后续使用维奈克拉再治疗时,部分患者仍可见效,但还需要深入研究来证实其疗效。
维奈克拉复用的疗效
一项使用维奈克拉联合利妥昔单抗治疗初诊CLL患者的Ⅰb期研究中位随访4.9年,18例患者在获得深度治疗反应后停止了维奈克拉的治疗。其中4例患者(2例MRD阳性CR,2例uMRD的CR)在停药后出现PD,随后研究人员对其使用维奈克拉或维奈克拉联合利妥昔单抗复治。在可评估治疗反应的3例患者中,所有患者均至少达到了部分缓解(PR),且有2例患者的治疗反应进一步加深。
MURANO试验的4年随访数据显示,维奈克拉联合利妥昔单抗治疗后有64例患者出现PD,其中14例继续接受维奈克拉或维奈克拉联合利妥昔单抗再治疗,其中11例可评估治疗反应的患者中总反应率(ORR)为55%。
笔记4:
对于既往未使用过共价BTKi治疗的患者,在维奈克拉治疗PD或复发后应考虑使用共价BTKi。
对于既往使用过共价BTKi且已知失败或耐药的患者,应考虑其他疗法。
共价BTKi的疗效
伊布替尼、acalabrutinib和zanubrutinib等共价BTKi改变了初诊和R/R CLL患者的治疗格局。
一项回顾性研究纳入了27例接受维奈克拉治疗后进展并使用伊布替尼继续治疗的患者。患者在维奈克拉治疗前接受的既往治疗中位线数为2线,12例患者存在del(17p)(12/20)、12例患者为复杂核型(12/24),13例患者为IGHV未突变(13/15)。18例患者因PD停止使用维奈克拉,经伊布替尼治疗后的ORR为56.0%(PR,13/25例;CR,1/25例)。
另一项单中心研究纳入了23例维奈克拉治疗后进展,并接受了BTKi(依鲁替尼或zanubrutinib)作为后续治疗的CLL患者,ORR达90%,PR或伴淋巴细胞增多的PR患者为15例,4例患者达CR。这些患者既往接受治疗的中位线数为4,且既往接受过氟达拉滨-环磷酰胺-利妥昔单抗(RFC)方案治疗的患者占91%,TP53缺失的患者占76%,复杂的核型患者占68%。
笔记5:
非共价BTKi在维奈克拉治疗后进展或复发的CLL患者中的疗效有待未来更多的临床研究数据证实。
非共价BTKi的疗效
伊布替尼(一种不可逆的共价BTKi)的耐药是由BTK中获得性半胱氨酸到丝氨酸突变介导的。GDC-0853、LOXO-305、ARQ 531和vecabrutinib等可逆的非共价BTK或可克服共价Ki耐药性。尽管非共价BTKi的临床试验正在进行中,尚处于早期阶段,既往接受过维奈克拉治疗的CLL患者应用缺乏确切的研究数据,但初步研究数据表明,这些药物在既往经过多线治疗的患者中具有临床活性。
LOXO-305的I期剂量递增临床试验的初步结果显示,维奈克拉治疗后具有获得性BCL2 Gly101Val突变的R/R CLL患者使用非共价BTKi治疗具有治疗反应。
笔记6:
目前的研究数据显示,PI3Ki在维奈克拉治疗后进展或复发CLL患者中疗效有限,疗效持续时间较短,且因副作用停药的患者比例偏高。
PI3K抑制剂(PI3Ki)的疗效
小样本的回顾性研究数据表明,PI3Ki在维奈克拉治疗后进展或复发的CLL患者中治疗活性有限,尤其是在BTKi和维奈克拉双重耐药的CLL患者中。
近期一项回顾性研究显示,使用维奈克拉治疗后进展或复发的17例CLL患者后续接受了idelalisib和duvelisib治疗,中位随访5个月时,ORR为46.9%,中位PFS为5个月,停药率为78%。值得注意的是,idelalisib和duvelisib已获美国食品药品监督管理局(FDA)批准用于R/R CLL患者治疗的临床试验,但并不包括对既往接受过维奈克拉治疗患者的后续治疗。
笔记7:
尽管在新药时代,我们对于Allo-HSCT在CLL患者中的应用疗效知之甚少,但其仍是CLL患者唯一可能治愈的方法。
另外,伊布替尼联合靶向CD19嵌合抗原受体(CAR)T细胞疗法可能有望成为既往接受过BTKi和维奈克拉治疗的R/R CLL患者的有效手段。
细胞治疗:异基因造血干细胞移植(Allo-HSCT)和CAR-T细胞疗法的疗效
近期的一项多中心回顾性队列研究显示,接受一种或多种新型药物治疗后经Allo-HSCT治疗的CLL患者在24个月时的PFS率为60%,OS率为82%。
在最大的国际多中心病例研究中,有18例接受了维奈克拉的治疗后进展或复发的CLL患者,这些患者既往都使用过BTKi,后续采用靶向CD19 CAR-T细胞疗法,ORR为66.6%,其中包括33.3%获得CR的患者。
2019年美国血液病学会年会上报道了CD19 CAR-T细胞产品lisocabtagene maraleucel(TRANSCEND-CLL-004)治疗R/R CLL(包括9例使用BTKi和维奈克拉治疗均失败)的研究,结果显示4例患者有持续治疗反应[3例PR,1例CR/CR且血液学恢复不完全(CRi)]。
另外,一项纳入既往经伊布替尼治疗失败进展的19例R/R CLL(包括11例既往接受过维奈克拉治疗)患者的研究显示,这些患者后续接受了CD19 CAR-T细胞联合伊布替尼治疗,尽管研究中没有单独评估既往接受维奈克拉治疗的患者结局,但整体患者的1年PFS高达59%。
本文总结了在维奈克拉治疗后进展或复发CLL患者的后续治疗选择(详见图1),以期指导临床实践。值得重视的是,分析停止维奈克拉治疗的原因以及明确既往的治疗方案是为该类R/R CLL患者选择后续治疗方案的关键。
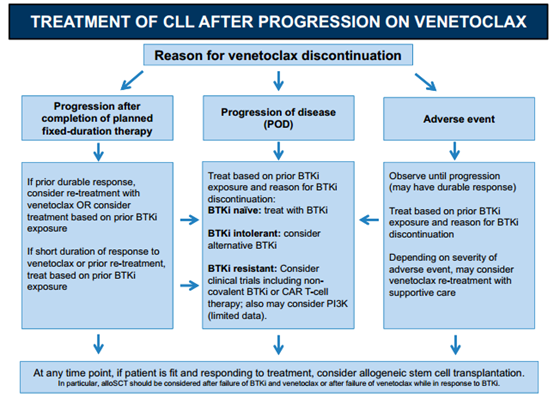
图1:基于Venetoclax的治疗进展后CLL的后续治疗选择推荐。
参考资料:
[1].Meghan C Thompson,Anthony R Mato.Treatment of relapsed chronic lymphocytic leukemia after venetoclax.Hematology Am Soc Hematol Educ Program.2020 Dec 4;2020(1):18-23.
[2].Kater AP,Seymour JF,Hillmen P,et al.Fixed duration of venetoclaxrituximab in relapsed/refractory chronic lymphocytic leukemia eradicates minimal residual disease and prolongs survival:Post-treatment follow-up of the MURANO phase III study.J Clin Oncol.2019;37(4):269-277.
[3].Kittai AS,Woyach JA.Resistance mechanisms to targeted agents in chronic lymphocytic leukemia.Cancer J.2019;25(6):428-435.