肝癌不同分期,该如何选择治疗方案?
肝癌的临床分期对于患者的预后判断及治疗方案选择至关重要。肝癌患者分期不同, 预后和治疗方案选择也大不同。国际上比较认同BCLC分期, 目前在国内, 我们较多地采用了2017版中国肝癌临床分期和BCLC分期系统及其治疗策略。最新2019年版肝癌分期方法请阅读文章:国家卫健委 | 原发性肝癌诊疗规范(2019年版) 全文,大致与2017年版相似。本文以2017年版肝癌分期为基础。
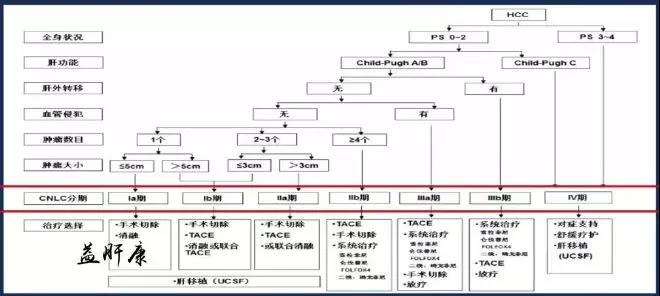
不同肝癌分期的治疗策略
早期肝癌的综合治疗策略
早期肝癌在2016版BCLC分期中是指BCLC 0-A期, 即肿瘤单发或多发肿瘤不超过3个, 最大径不超过3cm, 肝功能Child A-B期, PS评分为0。在2017版中国原发性肝癌诊疗规范中早期肝癌是指Ⅰa/Ⅰb期患者, 与BCLC分期类似。
治疗策略上, BCLC分期推荐手术切除, 肝移植和消融, 而2017版中国原发性肝癌诊疗规范推荐手术切除、肝移植、消融/+TACE, TACE。
术前诊断对于早期肝癌患者至关重要, 尤其是极早期肝癌。极早期肝癌是指肿瘤直径不超过2cm,即BCLC 0期患者。在这一阶段的肝癌, 影像学表现常常不典型, 术前要注意与肝硬化结节, 异性增生结节, 局灶增生结节, 肝腺瘤以及肝血管平滑肌脂肪瘤等良性肿瘤相鉴别。
其诊断要充分运用超声造影、核磁共振、CT、DSA、PET-CT/MRI等多种影像手段, 同时可选择肝细胞特异性的造影剂如钆塞酸二钠, 来提高肝癌诊断的准确率。临床诊断上可结合患者的年龄, 肝病基础, 影像学表现, 相关肿瘤标志物等结果进行综合判断分析。对仍不能确诊且存在肝癌高危因素的患者, 应果断采取肿瘤穿刺活检来明确诊断。
早期肝癌的治疗手段主要包括肝切除, 肝移植和局部消融治疗, 其中肝切除是首选治疗手段。
肝切除的手术方式有解剖性肝切除和非解剖性肝切除, 理论上应首选解剖性肝切除, 但受到患者肝功能、肝硬化情况和肿瘤位置的制约。如采取非解剖性肝切除应尽量保证切缘超过1 cm。
研究表明单发、最大径少于2 cm的肝癌患者接受解剖性肝切除和非解剖性根治切除的手术预后差别不大, 但肿瘤直径在2~5 cm的患者, 解剖性肝切除的局部控制效果更好, 抑制肝内转移的作用更明显。
肝切除手术目前有开腹和微创 (腹腔镜和机器人手术) , 微创技术的实施要根据患者的身体情况, 肿瘤位置, 肝硬化情况等综合判断, 在保证肿瘤根治的条件下有选择地实施。
2018年10月《新英格兰医学杂志》发表两篇MD安德森癌症中心的研究, 研究提示对早期宫颈癌患者开腹手术比腹腔镜/机器人手术更能让患者生存获益。因此这两种手术方式值得我们进一步研究。
此外有多种技术可辅助手术开展, 如吲哚菁绿15分钟滞留率评估肝脏储备功能, 三维可视化技术技术指导手术切除方案, 计算残肝体积, 吲哚菁绿荧光显像肿瘤示踪技术来探测肿瘤病灶。
研究表明肝癌患者术前采用三维可视化技术可优化基于二维成像技术制定的手术切除方案, 提高肝癌的根治切除率。
肝癌肝移植能提供比肝切除更高的5年生存率, 但花费巨大, 移植供体紧张且并发症发生率更高, 不作为常规选择。临床上, 推荐小肝癌合并肝硬化失代偿或者重度代偿期肝硬化患者首选肝移植。
局部消融治疗适用于单个肿瘤直径不超过5 cm, 或肿瘤数量不超过3个, 最大径不超过3 cm, 无血管、胆管及邻近器官以及远处转移。国内外多个肝癌临床治疗指南已将射频消融列为肝癌根治性治疗手段之一。多个报道显示其局部复发率较高, 远期生存率仍逊于肝切除。
目前推荐用于治疗小肝癌合并重度肝硬化或者肿瘤位置处于肝脏中心不适于或不愿意肝切除的患者。局部消融手段也要受限于肿瘤的位置, 肝硬化情况。对于那些临近胃肠, 胆囊, 大血管和胆管系统的肿瘤, 选择消融治疗要慎重。
消融的方式主要包括射频、微波、冷冻、激光、高功率超声聚焦和无水酒精注射等化学消融方式,可在超声、CT或者MRI等设备引导下操作, 操作途径包括经皮、腹腔镜和开腹3种方式。因此, 要根据肿瘤的大小、位置选择合适的影像引导设备、消融方式和操作途径。TACE联合射频消融能明显增加肝癌消融的疗效, 扩大了肿瘤消融的指征。
对于小肝癌不适于手术和消融治疗, 可考虑采用放射疗法, 已有研究报道小肝癌的放疗可达到和消融类似的治疗效果。
对于因预留肝体积不够而未能一期手术切除的患者, 可考虑行ALPPS或一期TACE+PVE, 二期肝切除的技术, 可提高手术切除率。
早期肝癌术后仍有较高的肿瘤复发转移率, 因此如何有效预防肝癌术后复发是手术切除后续关注的重点。
这里首先需要病理科医生对肿瘤标本的规范病理检测和结果解读。早期肿瘤生物学特性会导致手术预后有很大的不同, 需及时关注早期术后高危因素, 如微血管侵犯。针对高危复发因素的早期肝癌患者应做积极的抗复发治疗。
目前研究的结果提示乙肝相关肝癌患者术后接受抗病毒治疗、槐耳颗粒有一定的预防复发转移作用。少量研究也发现索拉菲尼对于伴有MVI的肝癌患者手术后有一定的预防复发作用。而目前上市的新的靶向药物如仑伐替尼、瑞戈非尼、卡博替尼、阿帕替尼、PD-1/PD-L1抑制剂等, 其预防复发作用仍有待临床试验结果证明。
中期肝癌的综合治疗策略
中期肝癌是指BCLC B期, 中国肝癌分期Ⅱa/Ⅱb期。
BCLC分期推荐TACE治疗, 而2017版中国肝癌诊疗规范推荐手术切除、TACE和全身治疗 (索拉菲尼/FOLFOX4) 。相较于BCLC分期, 我国, 日本和亚太指南则推荐有选择地行手术切除。手术切除在中期肝癌治疗中仍占有举足轻重的地位。一项随机对照研究结果显示中国Ⅱa期患者手术切除地生存获益要优于TACE。
肝癌术前的辅助治疗主要是TACE。对于可切除的肝癌术前辅助TACE治疗是否让病人获益仍存在争议。
有研究表明术前辅助TACE肿瘤有反应组的患者手术总体生存率和无瘤生存率均高于对肿瘤无反应组, 提示影像学表现为富血供的多发肝癌可在术前采取辅助TACE治疗, 而乏血供的肝癌患者则不推荐术前TACE。有较多研究表明肝切除术后辅助TACE治疗能推迟肿瘤复发, 延长患者的生存时间, 特别是那些手术切除后高危复发的人群获益更大。但术后辅助TACE的治疗指征, 化疗药物的选择, 介入次数等方面缺乏统一的规范, 尚需要大量临床研究进一步明确。少量研究表明针对BCLC B期患者, 手术联合索拉非尼治疗效果优于单纯手术, 显著延长肝癌患者的术后生存时间。
不能手术切除的中期肝癌患者的首选治疗方法是TACE。但对于化疗药物和栓塞剂的选择仍没有最佳推荐, 需要介入科医生继续摸索。研究表明钇90放射介入治疗能显著提高疗效, 延长患者生存时间。TACE联合碳酸氢钠能增加肿瘤的反应率, 提高TACE的疗效。另外研究也发现TACE联合索拉非尼能显著延长BCLC B期患者的生存时间。
晚期和终末期肝癌的综合治疗策略
晚期肝癌是指BCLC C期或者中国肝癌分期Ⅲa/Ⅲb期。
BCLC分期推荐唯一标准治疗索拉非尼, 2017版中国肝癌诊疗规范推荐全身治疗(索拉菲尼/FOLFOX4) 、TACE、放疗和手术切除。注:2019年版的中国《肝癌诊疗规范》对Ⅲa/Ⅲb期患者治疗新增一线药物仑伐替尼,二线药物瑞戈非尼;2018年版中推荐一线索拉非尼和仑伐替尼为,二线瑞戈非尼、纳武单抗和派姆单抗(I级证据)、卡博替尼和雷莫芦单抗(II级证据)。
此期的肝癌患者肿瘤情况比较复杂, 类型不同, 治疗方案也大不同。近年来, 肝癌的靶向药物也有更新。仑伐替尼, 瑞戈非尼, 卡博替尼、阿帕替尼、PD-1/PD-L1抑制剂等均表现出治疗肝癌的作用。
由于此期的患者血液里的循环肿瘤细胞最多, 因此有效的靶向药物治疗是提高其它局部治疗手段的关键步骤。FOLFOX4化疗方案被证明比传统阿霉素化疗方案更能使晚期肝癌患者生存获益, 目前缺乏其与索拉非尼的头对头研究, 在临床应用有限。
Ⅲa期患者肿瘤仍局限于肝内, 伴脉管侵犯, 主要是指门静脉, 肝静脉或胆管侵犯。肝癌合并胆管癌栓, 肿瘤如果可切除, 应尽量采取手术切除。肿瘤如不可切除, 则可选择TACE, 放疗, 胆管支架或胆道消融等局部治疗, 缓解病情。
肝癌合并门静脉癌栓的患者, 要根据门静脉癌栓的范围和肿瘤的情况进行具体分析, 一般对于门静脉癌栓程氏分型Ⅰ、Ⅱ型, 肿瘤可切除, 肝脏储备功能较好, 考虑手术完整切除癌栓和肿瘤, 同时术后联合TACE, 索拉菲尼等靶向药物治疗。对于门脉癌栓处于程氏分型Ⅲ、Ⅳ型的, 完整切除癌栓的代价太高, 可建议行局部放疗, TACE和靶向药物进行降期治疗, 寻求手术机会。
对于肝癌合并肝静脉癌栓的原则上同门静脉癌栓。手术过程中应提前做好向心血流阻断, 避免癌栓脱落导致栓塞。
对于Ⅲb期患者, 一般不建议手术治疗。但有些特殊情况值得我们进一步研究和商榷, 如肝外转移为可切除的单器官孤立或少量转移灶。类似于肠癌肝转移, 手术切除联合靶向药物治疗是否能有更好效果, 这需要临床试验来验证。
终末期肝癌是指BCLC D期或中国肝癌分期Ⅳ期。此期的肝癌患者身体状况或者肝功能状态不能承受强烈的抗肿瘤治疗, 如手术, TACE, 放疗, 靶向药物, 化疗等, BCLC和中国肝癌诊疗规范均推荐对症支持治疗。有一类特殊的终末期肝癌患者, 早期肝癌合并肝功能Child C级, 应该积极地接受肝移植手术。