非小细胞肺癌术后EGFR-TKIs治疗研究进展
手术被认为是非小细胞肺癌(NSCLC)的主要治疗选择,然而只有25%~30%的患者能做根治性切除,5年生存率在从Ia期到IIIa期介于67%和23%之间,部分II期和III期NSCLC患者仍将死于疾病复发。术后辅助治疗的目的就是消灭微转移,延缓复发。目前术后辅助治疗的标准方案为以铂类为基础的两药化疗4周期。表皮生长因子受体(EGFR)突变检测近年来不但被推荐用于指导患者选择表皮生长因子受体-酪氨酸激酶抑制剂(EGFR-TKIs)治疗,而且也作为一种术后常规检查,尤其是在中国的NSCLC患者中。伴有EGFR突变的晚期肺腺癌患者已被证实能从TKIs的治疗中获益,TKIs也越来越多地作为术后辅助治的主要手段。本文就近年来NSCLC术后EGFR-TKIs治疗的研究进展作如下综述。
01术后EGFR-TKIs治疗效果
一些研究认为EGFR-TKIs靶向治疗在NSCLC术后的辅助治疗中无明显优势(表1)。一项来自加拿大的试验BR19对完全切除的NSCLC患者按分期、组织学类型、性别、是否接受术后放疗和化疗进行随机分配(1∶1),使两组基线因素得到平衡,分别给予两组患者吉非替尼每日250 mg或安慰剂2年。结果发现无病生存期(DFS)和总生存期(OS)均无获益,即使是在15名EGFR突变阳性的患者中仍得到相同结论,KRAS突变亚组分析结果甚至安慰剂组生存有更好的趋势。因该试验提前终止,最终入组的患者仅达到试验预设样本量的40%,导致检验效能不足。而且该研究未将EGFR突变进行分层,对化疗是否有益仍有争议的Ib期患者占总人数的51.7%,因此难以得到可靠的结论。美国的Janjigian YY等回顾性分析了167例EGFR敏感突变的术后患者(Ib期占70%,II期占15%,IIIa期占15%),结果显示TKIs治疗的患者2年DFS有获益的趋势,而OS在两组间差异无统计学意义。由于该研究为回顾性研究,两组之间基线因素未平衡,因此结论具有局限性。SELECT试验在EGFR敏感突变的NSCLC患者接受术后标准辅助治疗(化疗或化放疗)后,接受厄洛替尼150 mg/天持续两年,2年DFS为85%,这与未接受厄洛替尼治疗的术后患者的历史数据76%相比,有明显获益。然而由于这是一项单臂研究,缺少对照组,难以为术后TKIs治疗提供有力证据。RADIANT[9]是在NSCLC术后患者中,以厄洛替尼150 mg每天一次持续两年与 安慰剂作对照,发现DFS差异无统计学意义。161例 EGFR阳性患者中,厄洛替尼组DFS有获益的倾向,但在统计学上不显著。由于该研究时间较早,判断EGFR阳性的方法采用了免疫组化(IHC)和荧光原位杂交(FISH),IHC检测EGFR蛋白表达与FISH不能预测EGFR敏感突变,因此造成结果不准确。
表1 术后EGFR-TKIs治疗的相关研究
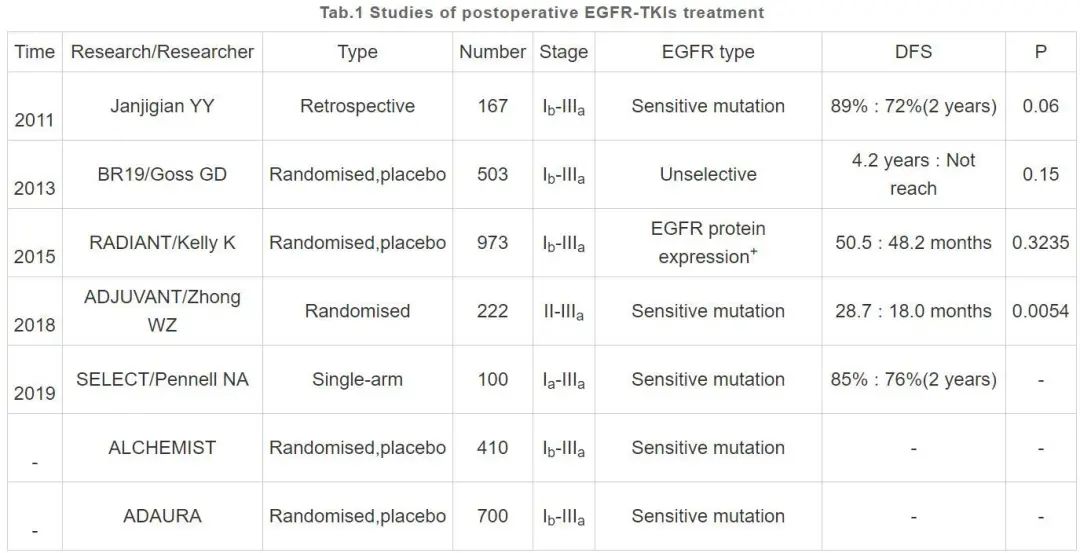
由于这些研究存在着许多的局限性,很多学者又重新评估了术后辅助TKIs的治疗效果(表1)。一项国内的研究ADJUVANT对比了吉非替尼与化疗(长春瑞滨加顺铂双药方案)在EGFR敏感突变的术后患者中的疗效,吉非替尼组的中位DFS明显长于化疗组。其中pN2亚组的获益更多,pN1亚组获益不明显。但ADJUVANT不足之处便是OS数据尚未成熟。而正在进行的ALCHEMIST(NCT02193282)和ADAURA(NCT02511106)试验有助于确定TKIs的OS获益。在ALCHEMIST中,EGFR突变/ALK基因重排的患者在完成术后标准辅助化疗后,将随机分为安慰剂组和厄洛替尼/克唑替尼组。ALCHEMIST还将为基因组研究提供机会,以充分了解基因的构型和演变以及耐药机制。ADAURA是EGFR敏感突变的非鳞癌NSCLC术后患者1∶1随机分成两组,分别接受奥希替尼80 mg/天和安慰剂。这项或许将在2021年得出结果的研究不但分析了TKIs对生存的影响,还探索性地研究了奥希替尼在基线T790M突变的患者中的疗效。
02术后EGFR-TKIs治疗的毒性反应与安全性
尽管大多数患者对EGFR-TKIs的耐受性良好,仍然会有一些患者因各种毒性反应而终止TKIs治疗。临床上最常见的毒性反应包括皮肤毒性反应和腹泻,而间质性肺炎是少见但是较危险的毒性反应。各个TKIs之间的毒性反应也存在差异。一项纳入16个试验共2 535例突变或野生型EGFR患者的荟萃分析比较了TKIs与化疗/安慰剂在毒性反应上的差异,毒性相关死亡并不多见(1.7%),40%患者发生了Ⅲ/Ⅳ级毒性反应。最常见的毒性反应包括腹泻和皮疹,且阿法替尼较吉非替尼和厄洛替尼更容易发生这两个毒性反应,而吉非替尼转氨酶升高较其余二者更常见。对于第三代的奥希替尼,一期AURA临床试验表明,与其他经批准的EGFR TKIs的历史数据和临床经验相比,奥希替尼有更少的皮肤和胃肠道毒性。
现有的研究认为在术后的患者中使用EGFR-TKIs也是可耐受的。最早是一项来自日本的研究计划将吉非替尼用于完全切除的术后患者,由于日本报道了越来越多的晚期NSCLC患者在应用TKIs时出现了间质性肺炎,该研究中途停止。通过对入组的38例患者进行分析,研究者未发现术后4~6周给予吉非替尼对手术相关并 发症的影响。RADIANT试验中,厄洛替尼组有2.5%的患者发生药物相关的严重毒性反应,安慰剂组为1.5%。没有治疗相关的死亡发生。毒性反应导致的永久性停药发生率在厄洛替尼组和安慰剂组分别为 33.6%和2.6%。ADJUVANT试验吉非替尼组与化疗组毒性反应发生率分别为58%和80%,严重毒性反应发生率分别为7%和23%,可见吉非替尼较化疗有减小毒性反应的趋势。Xie等人的研究回顾性分析对比了吉非替尼与化疗在术后患者中的疗效与毒性反 应,吉非替尼组最常见的毒性反 应为皮疹(76.9%)、转氨酶升高(53.8%)、腹泻(46.2%),而化疗 组最常见的毒性反应为中性粒细胞 减少(67.3%)、恶心呕吐(63.5%)、贫血(44.2%)。其中Ⅲ级以上毒性反应在吉非替尼组与化疗组分别 为15.4%和38.5%。吉非替尼治疗3个月后,1例患者被诊断为肺间质性疾病。无治疗相关死亡发生。可见无论是毒性反应总的发生率还是严重毒性反应发生率,TKIs均较化疗有所减小,但是TKIs导致的肺间质性疾病还应该引起足够重视。
03术后EGFR-TKIs治疗的争议与未来研究方向
3.1 术后TKIs治疗时间
目前大多数研究使用TKIs的时间为两年,这是根据II-III期亚组患者术后的中位DFS以及既往TKIs的研究数据所确定的。N1期21个月左右复发,N2期9~10个月复发,因此将用药时间设定为超过中位DFS的两年。另外,从伊马替尼得到启示,有研究表明伊马替尼治疗时间延长对于晚期胃肠道间质瘤(GIST)的治疗有明显获益,推荐持续服用伊马替尼一直到病情进展。Joensuu H等[19]的研究发现与12个月的术后辅助伊马替尼相比,36个月的伊马替尼改善了GIST复发高危患者的无复发生存率(RFS)和总生存率。但目前缺乏相关研究将该结论推论至NSCLC术后TKIs治疗。
而相较于仅仅3个月左右的辅助化疗,是否可以缩短辅助TKIs的治疗时间也需要进一步研究。一项正在进行的临床II期试验BD-IC-IV50预计纳入120例EGFR敏感突变的IIa-IIIa期术后患者,两组分别应用埃克替尼1年和2年,对RFS进行对比分析。我们期待研究结果为术后TKIs应用时间带来新的证据。
3.2 术后TKIs治疗人群选择
EGFR突变是术后TKIs治疗有效的必备条件。除了EGFR基因外,还有一些伴随基因异常也会影响TKIs在NSCLC患者中的疗效。复旦大学附属中山医院的一项前瞻性研究纳入了51例存在EGFR敏感突变的NSCLC局部晚期或晚期的患者,发现伴随基因异常发生率最高的依次为TP53基因(55%)、EGFR基因扩增(26%)、RB1基因(18%),其中TP53基因和RB1基因突变的患者接受EGFR-TKIs治疗的无进展生存期(PFS)显著短于无突变的患者。Kim Y等回顾性分析了伴随基因异常对TKIs疗效的影响,研究显示TP53、RB1、PTEN以及 MDM2 都与更差的PFS相关。这些基因改变会导致患者TKIs原发性耐药,因此在考虑为EGFR突变的术后患者选择合适的辅助治疗时,也应该在目前的基因常规检测中加入更多的检测位点。
在可切除的NSCLC患者中,多发淋巴结转移是常见的预后因素,这部分患者在根治术后极易复发与转移。辅助化疗已被证实对II-IIIa期患者有好处,但对Ib期患者则不建议常规使用。先前的研究大多选择Ib-IIIa期的患者且Ib期患者数较多,因此未得出TKIs有效的结论。考虑到N1或N2患者与N0患者相比预后较差,他们更可能从长期辅助治疗中获益,因此ADJUVANT仅纳入N1和N2患者。还有一种理论认为EGFR通路在疾病早期发挥的作用较小,早期肿瘤并不像晚期肿瘤那样依赖该通路作为致癌驱动因素。而对于IIIa-N2期,目前推荐标准辅助化疗方案后再给予术后放疗(PORT)。若在EGFR敏感突变的人群中用术后TKIs治疗取代化疗,PORT是否仍能改善患者的生存也是将来需要探讨的问题。
3.3 术后TKIs治疗的继发性耐药与复发
对于术后辅助应用TKIs的一个担忧就是治疗本身就会诱导产生继发性耐药基因突变。EGFR-TKIs的继发性耐药类型可大致分为以下几种:EGFR二次突变(如T790M突变);交替信号通路的激活(如MET基因扩增,HER-2扩增);下游通路改变(如KRAS继发性突变,PIK3CA继发性突变);其他机制包括一些表型的改变(如EMT、NSCLC变成SCLC)[25]。SELECT中对40例复发患者再次进行活检,仅发现1例T790M突变,且多数复发患者再次使用TKIs仍能带来一定获益。因此,对于复发的患者,鼓励其再次行组织活检,根据病理及分子特征进行针对性治疗。
第三代TKIs就是针对第一、二代TKIs耐药患者而应用于临床的,奥希替尼通过靶向位于密码子797(C797)的半胱氨酸残基与EGFR激酶不可逆结合,具有高度选择性的抑制活性。然而对奥希替尼的耐药机制已经得到证实,40%的T790M阳性患者中发现了EGFR C797S突变,该突变阻断了药物的结合。有研究表明,对T790M 和C797S定位有助于确定下一步治疗策略。当C797S和T790M突变在不同等位基因时,耐药细胞对第一代TKIs联合第三代TKI敏感;当C797S和T790M在同一等位基因时,所有TKIs均无效。
对于术后患者,在TKIs辅助治疗复发后也仍可以根据基因检测来选择靶向药物,或者选择传统的放化疗,未来还有可能将免疫治疗联合靶向治疗用于NSCLC患者。
结语
目前的研究可以看出EGFR-TKIs对于NSCLC术后的患者是有效且可耐受的,TKIs与化疗相比为患者带来更好的生存率与更少的毒性反应,且在复发后仍然有多种方案可选。尽管现有的研究OS数据尚不成熟,我们期待后续的研究为TKIs术后辅助治疗带来更加充分的证据。而且随着更详细的基因位点检测和更多具有针对性的靶向药的研发[30],EGFR突变的患者将会有更多个体化的治疗方案,使其生存期得到延长,生活质量得到改善。