CD8+T细胞:所有您想知道的
T淋巴细胞(T lymphocyte)在构成适应性免疫基础的细胞介导过程中起着至关重要的作用。幼稚T细胞上的T细胞受体(T cell receptor,TCR)识别与主要组织相容性复合体(majorhistocompatibility complex,MHC)I类蛋白结合的特异性抗原时,它们成熟并增殖为执行关键免疫功能的T细胞类型的专门子集。在本文中,我们通过表征CD8+T细胞的免疫表型和细胞介导的免疫功能背后的过程,来认识CD8+T细胞。
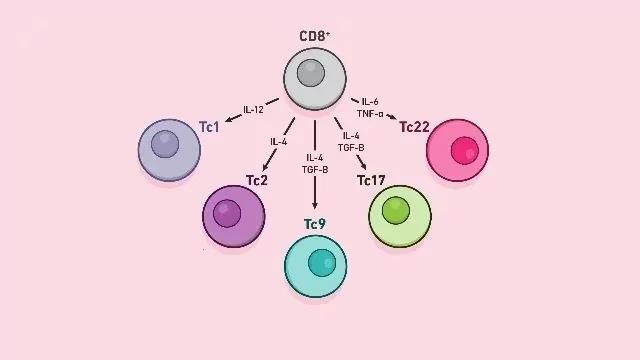
什么是CD8+T细胞?
被称为细胞毒性T淋巴细胞(cytotoxic Tlymphocyte,CTL),CD8+T细胞属于在其表面表达CD8的亚群。CD8是一种二聚体共受体,可使CD8+T细胞识别MHC I类蛋白呈递的肽。
❄MHC I类与MHC II类有什么区别?
主要的组织相容性复合体(MHC)是DNA区域,其中包含许多基因,这些基因编码所有有核细胞在其表面表达的糖蛋白分子。MHC分子有两大类。它们之间有关键区别。
MHC I类分子在生物体中所有有核细胞的表面表达。它们在“自身”抗原的呈递中起着至关重要的作用。当细胞被细胞内病原体(例如病毒)感染时,MHC I类蛋白将发生变化,向自然杀伤(NK)细胞指示该细胞需要被破坏。
MHC II级分子仅由称为抗原呈递细胞的免疫细胞亚群表达。MHC II类识别通过向淋巴细胞(例如CD4+辅助T细胞)发出信号,对于启动适应性免疫应答至关重要。
幼稚的CD8+T细胞与抗原呈递细胞(Antigen-presentingcells,APC)之间的成功结合会刺激未成熟的T细胞成为具有细胞毒性功能的活化CD8+T细胞。具有杀伤细胞内病原体和肿瘤细胞等细胞毒性能力,CTL属于一组参与细胞介导的适应性免疫的专门淋巴细胞。虽然CTL对功能性免疫系统必不可少,但CTL的失调可导致器官特异性自身免疫性疾病的发病,如糖尿病或关节炎。
CD8+T细胞起源于何处?
所有T细胞均起源于从骨髓迁移至胸腺的淋巴样祖细胞。胸腺容纳尚未成熟的T细胞,尚未发育出抗原识别所需的T细胞受体。在感染过程中,最初的CD8+T细胞最初是通过与淋巴器官内的APC相互作用来刺激的。
CD8+T细胞发育
一旦未成熟的T细胞迁移到胸腺,它们就准备发展成CD8+细胞。祖T淋巴细胞首先经历了许多DNA重排,这些重排产生了多种TCR,这些TCR能够识别来自外源或细胞内病原体的抗原。TCR多样性取决于TCR基因的随机DNA重排数目,这些重排导致独特的抗原特异性受体的表达。一旦确定了CD8之类的TCR功能稳定,未成熟的T细胞就准备好进行称为克隆选择的抗原介导过程。当TCR与胸腺细胞呈递的MHC I类蛋白质复合时,抗原结合抗原时,便开始进行阳性选择。如果该结合事件对于CD8成功,则新激活的CD8+T细胞将继续分化为成熟的CTL。在此阶段无法与抗原-MHC I类复合物充分结合的未成熟T细胞将发生凋亡。当未成熟的T细胞与自身抗原的结合太强时,就会发生阴性选择。对阴性选择的T细胞进行编程以使其发生凋亡,从而消除了它们对健康细胞进行自身反应的能力。
CD8+T细胞活化
经历阳性选择的幼稚CD8+T细胞需要额外的信号传导过程来确定其命运。例如,CD4+辅助性T细胞可以调节APC,以向幼稚CD8+T细胞提供更强的抗原信号。辅助性T细胞或树突状细胞(dendriticcell,DC)也可以通过共刺激信号(例如CD80/86以及细胞因子IL-12)介导细胞毒性T细胞活化。使用共刺激性T细胞辅因子同时激活TCR,可使激活的CD8+T细胞增殖为包含效应和记忆T细胞类型的扩展群体。阳性选择的CD8+T细胞向高度特异性CTL的扩增是克隆选择的最后一步。
细胞毒性T细胞有什么作用?
一旦CD8+T细胞被激活,它们将经历一连串的复制和分化步骤,从而引发它们的定向免疫应答。与靶向感染或恶性细胞物理接触的CTL诱导凋亡,这是一种通过细胞毒性酶和分子进行的程序性细胞死亡形式。
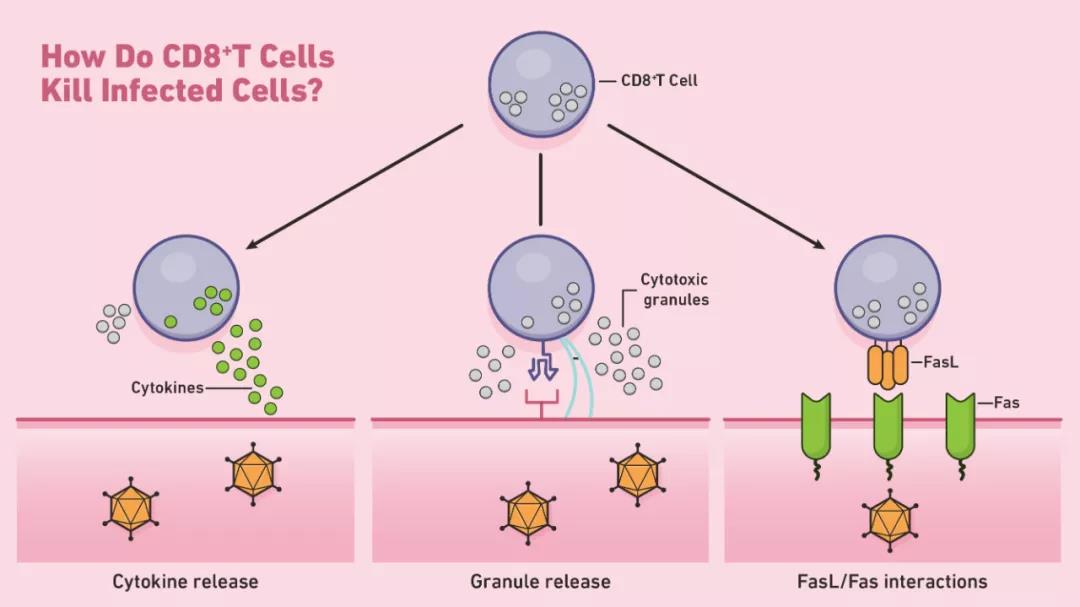
CD8+T细胞如何杀死感染的细胞示意图。
CD8+T细胞启动凋亡的一种方式是通过穿孔素和颗粒酶(两种类型的细胞毒性蛋白)的分泌。穿孔素是在靶细胞的细胞膜上形成孔的溶细胞蛋白。CTL使用这些孔来引导粒酶的释放,粒酶是一类丝氨酸蛋白酶,可继续在细胞质内凋亡。这些蛋白酶通过裂解参与正常细胞维持的病毒和细胞蛋白来关闭靶细胞。然后,经历凋亡的靶向细胞被附近的吞噬细胞清除。CTL还可以通过Fas-Fas配体相互作用诱导细胞凋亡。每当Fas配体(Fas ligand,FasL)与靶细胞上的Fas受体结合时,一系列信号分子就会通过激活半胱天冬酶蛋白酶(cysteinyl aspartate specific proteinase,含半胱氨酸的天冬氨酸蛋白水解酶)来启动细胞凋亡。这些蛋白酶在细胞凋亡的后期进行大部分的蛋白水解。
除定向凋亡外,CD8+T细胞还可以通过释放诸如TNF-α的细胞因子来间接杀死靶细胞。例如,类型1 CD8+T细胞(Tc1)可以释放IFN- γ ,这是一种能够抑制病毒复制并增强特定抗原呈递的细胞因子。在其主要反应结束时,活化的CD8+T细胞通常会因凋亡而死亡。
CD8+T细胞亚型
分化为效应细胞或记忆细胞类型的幼稚CD8+T细胞发挥特定作用,介导适应性免疫反应。诱导成为效应细胞的T细胞分化为Tc1或Tc2细胞。Tc1细胞一旦受到细胞因子(例如IL-2和IL-12)的刺激,便具有直接或间接杀死目标细胞的能力。另外,具有细胞毒性的Tc1细胞可以释放IFN- γ或TNF-α,以进一步调节宿主的免疫反应。Tc2 T细胞通过分泌细胞因子IL-4,IL-5,IL-10和IL-13来调节效应免疫和辅助免疫反应。尽管Tc2细胞具备执行细胞毒性功能的能力,但在感染过程中,这种T细胞亚群通常不如其Tc1对应物有效。
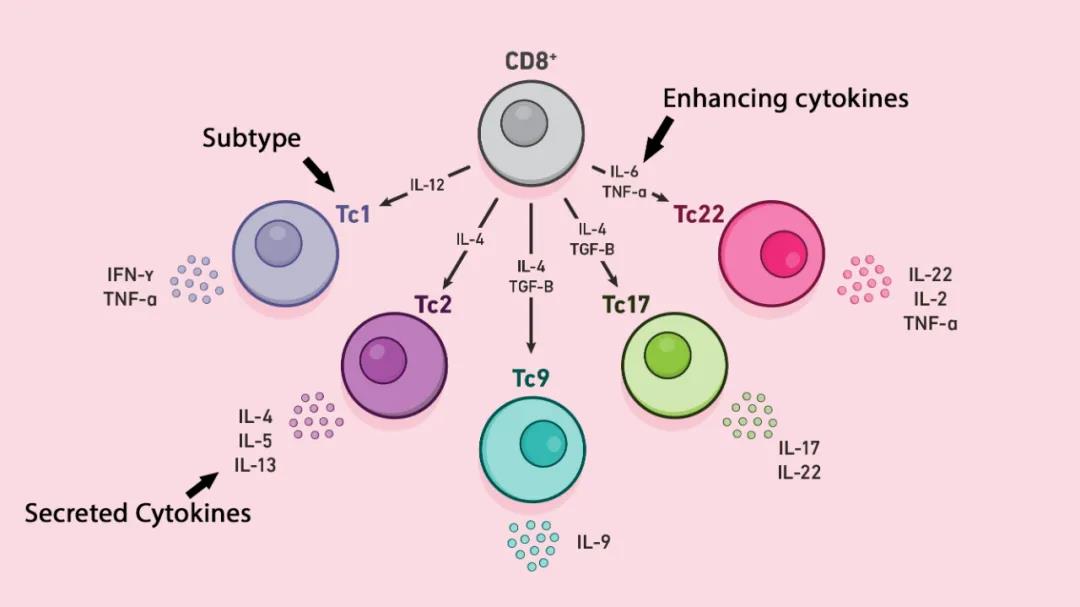
CD8 + T细胞亚型包括Tc1,Tc2,Tc9。Tc17和Tc22。
CD8+T细胞的记忆子集可分为三类:中央记忆细胞,效应记忆细胞和组织驻留记忆细胞。这些子集的特征在于其功能、增殖能力和位置的差异。中央记忆细胞(Tcm)是驻留淋巴细胞的淋巴细胞,通过快速增殖对继发感染作出反应。在人类中,Tcm细胞的表型特征在于它们共同表达表面标记CD127、CD27和CD28。效应记忆细胞(Tem)在全身循环,准备寻找并杀死与抗原匹配的靶细胞。与它们的Tcm对应物不同,这些效应记忆细胞在感染后并未表现出强大的增殖或自我更新能力。
CD8+与CD4+T细胞
CD4+淋巴细胞是一组“辅助” T细胞,它们通过直接和间接机制介导其他免疫细胞活性。幼稚的CD4+T细胞驻留在胸腺中,直到被表达其靶抗原结合的MHC II类蛋白的APC刺激。这种蛋白复合物的成功结合激活了CD4+T细胞,开始分化为辅助细胞类型。即使激活的CD4+T细胞不像CD8+T细胞那样执行细胞毒性功能,它们也会成熟为辅助T细胞类型,可以通过分泌细胞因子介导体液或细胞介导的免疫反应。
|
比较 |
CD8+T细胞 |
CD4+T细胞 |
|
类型 |
细胞毒性或“NK”细胞 |
“辅助”类细胞 |
|
关键功能 |
消灭恶性细胞感染 |
介导免疫细胞活性 |
|
TCR-MHC结合复合物 |
CD8+MHC I类 |
CD4+MHC II级 |
|
子类型数 |
五 |
六 |
CD8+T细胞在哪里适合更广泛的免疫反应?
CD8+T细胞调节取决于TCR介导的刺激和抑制机制的集合。当CD8+T细胞呈递其特异性抗原时,它们会经历众多克隆扩增,产生适应性免疫应答所需的分化细胞类型。与通过TCR呈递抗原无关,CD8+T细胞可以通过细胞因子的分泌间接攻击病原体或肿瘤细胞。然而,不受控制的CTL活性可能有助于针对健康细胞的自身免疫反应。在这种情况下,对CD8+T细胞过程的更多了解可以增强我们设计有效疫苗或实时操纵细胞介导的免疫反应的能力。
参考文章:
1.Zhang, N, Bevan, MJ. CD8+T cells: Footsoldiers of the immune system. Immunity. 2011;35(2):161-168.doi: 10.1016/j.immuni.2011.07.010 2.Deng Q, LuoY, Chang C, Wu H, Ding Y. and Xiao R. The emerging epigenetic role of CD8+Tcells in autoimmune diseases: A systematic review. Front. Immunol. 2019;10:856.doi: 10.3389/fimmu.2019.00856 3.Hoyer S,Prommersberger S, Pfeiffer IA, Schuler-Thurner B, Schuler G, Dörrie J, SchaftN. Concurrent interaction of DCs with CD4(+) and CD8(+) T cells improvessecondary CTL expansion: It takes three to tango. Eur. J. Immunol.2014;44(12):3543–59.doi: 10.1002/eji.201444477 4.Tau G,Rothman P. Biologic functions of the IFN-γ receptors. Allergy. 1999;54(12):1233–1251.doi: 10.1034/j.1398-9995.1999.00099.x 5.Zhu J, PaulWE.(2008). CD4 T cells: fates, functions, and faults. Blood.2008;112(5):1557–69.doi: 10.1182/blood-2008-05-078154 6.Berg RE,Forman J. The role of CD8 T cells in innate immunity and in antigennon-specific protection. Curr Opin Immunol. 2006;18(3):338-343.doi: 10.1016/j.coi.2006.03.010