伊立替康不良反应
拓扑异构酶Ⅰ诱导可逆性 DNA 单链断裂,从而使 DNA 双链结构解螺旋,参与 DNA 复制过程。伊立替康(CPT-11)及其活性代谢产物 SN-38 可与拓扑异构酶Ⅰ-DNA 复合物结合,阻止断裂单链的再连接,对 DNA 产生不可逆损伤,最终导致细胞死亡。CPT-11 为细胞周期特异性药物,特异性作用于 S 期。
CPT-11 主要不良反应包括:胆碱能综合征、迟发性腹泻、中性粒细胞减少。上述不良反应发生的时相见图 1。
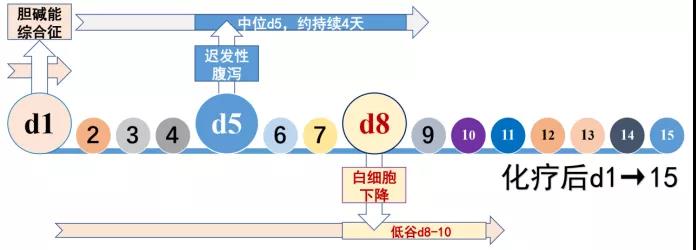
图 1:伊立替康化疗给药后主要不良反应发生时相示意图(图源:作者)
伊立替康主要不良反应各论
01 乙酰胆碱能综合征
发生机制:伊立替康是乙酰胆碱酯酶的非竞争性抑制剂,可抑制胆碱酯酶活性,使体内乙酰胆碱积聚,该特性与用药后出现的乙酰胆碱能综合征相关。
临床表现:用药后 24 小时内出现的下述症状称急性乙酰胆碱综合征:早发性腹泻、出汗、流涎、视力模糊、腹痛、流泪等。
治疗措施:使用硫酸阿托品治疗(0.25 mg 皮下注射),有禁忌症者除外。对哮喘的患者应小心谨慎。
预处理:
对有急性、严重的胆碱能综合征患者,下次使用本品时,应预防性使用硫酸阿托品。
首剂及随后每次伊立替康给药前,给予阿托品皮下注射行预处理的临床也较常见。
02 迟发性腹泻
发生机制:伊立替康活性代谢产物 SN-38 在肠道内的浓度及其与肠道上皮接触的时间是导致迟发性腹泻的关键。其可引起 DNA 断裂,使肠道上皮细胞坏死、凋亡,导致水、电解质吸收障碍及液体过度分泌。
肠道内的羧酸酯酶参与伊立替康向 SN-38 的转化。肠道细菌的 β-葡萄糖苷酸酶也可将无活性 SN-38 G 转化为 SN-38。
肝和肠内的代谢酶 UGT1A1 可将活性 SN-38 代谢为醛酸化灭活产物 SN-38 G,从而减少不良反应。UGT1A1 是决定肠内 SN-38 浓度和肠毒性大小的关键,UGT1A1 基因的多态性可导致该酶活性的差异,影响药物分布和代谢,进而产生不同程度的腹泻症状。
UGT1A1 基因检测:UGT1A1 基因检测有助临床预判不良反应强度,包括肠道反应、血液毒性等。
其中 UGT1A16、UGT1A128 等突变可导致 SN-38 葡萄糖醛酸化减少,SN-38 在体内蓄积,进而毒性增加,诱发严重腹泻。UGT1A128 纯合突变患者,建议伊立替康减量 30% 以避免严重不良反应。UGT1A16 多态性对伊立替康毒副反应的预测意义同样重要,其仅在亚洲人群发现,国内通常将 UGT1A16 与 UGT1A128 同时检测。
但即使减量使用伊立替康,UGT1A16 和 UGT1A128 纯合突变仍为迟发性腹泻、粒细胞减少的高危因素,这部分患者也可考虑选择其他替代化疗药物。
此外,UGT1A1 野生型患者仍有发生迟发性腹泻的可能。
原因在于,伊立替康导致迟发性腹泻的机制较为复杂,除上述 UGT1A1 基因多态性外,其他如:转运体 OATP1B1 的基因多态性降低其对 SN-38 转运能力,导致 SN-38 在胃肠道暴露而引发胃肠道毒性;或联合替吉奥化疗;或伊立替康致前列腺素 E2(PGE2)升高,诱发肠上皮细胞氯离子分泌增加、钠离子吸收减少,导致腹泻;或伊立替康破坏肠道紧密结合蛋白导致腹泻等,也可参与迟发性腹泻的病理过程。
临床表现:使用伊立替康 24 小时后出现的药物相关性腹泻,为剂量限制性毒性,无蓄积性,表现为大便次数增加,大便性状改变,出现溏稀便、水样便等,可伴腹痛、腹胀不适及乏力、虚弱感等。
迟发性腹泻发生的中位时间一般为化疗后第 5 天,与给药方案相关,平均持续约 4 天。发生率可达 90%,3~4 级占 39%。
治疗措施:
提前告知患者腹泻风险,早发现、早干预。
止泻、补液、防治电解质紊乱等。
治疗其他并发疾病,尤其合并中性粒细胞减少的患者,警惕严重肠道感染及死亡风险,积极联合抗感染等治疗。
03 化疗后骨髓抑制
发生机制:化疗药物对生命周期短、更新生长活跃细胞的非选择性打击。
UGT1A1 基因检测:UGT1A1 基因检测有助临床预判血液毒性严重程度。
临床表现:化疗后查血常规示白细胞、中性粒细胞减少,也可见血红蛋白、血小板等下降。单药/联合化疗中,到粒细胞最低谷的中位时间一般为 8-10 天。
治疗措施:
- 治疗期间合理监测血细胞计数。
- 药物治疗,如升白针的运用。
- 粒细胞减少伴发热,应收治入院,予抗感染治疗。
- 警惕粒细胞减少合并腹泻、肠道感染。
- 曾发生严重血液学毒性的患者,后续治疗周期可考虑减量。