SENIOR研究:≥80岁DLBCL患者R2-miniCHOP治疗并不优于R-miniCHOP
SENIOR研究是一项III期随机研究,比较≥80岁新诊断的DLBCL患者采用R2-miniCHOP方案与R-miniCHOP方案治疗的耐受性和有效性。结果显示,R2-miniCHOP没有改善患者生存,而且会增加不良事件,因此对≥80岁新诊断的DLBCL患者需要新的治疗策略。
研究背景
弥漫大B细胞淋巴瘤(DLBCL)是最常见的淋巴瘤亚型,发病率随着年龄增长而增加。约40%的DLBCL患者年龄大于70,即使经CD20抗体联合化疗进行治疗,新诊断的老年DLBCL患者预后仍较年轻患者差,合并症和生理器官功能下降常常导致难以控制的治疗毒性并因此限制了最佳化疗方案的应用。
二项II期研究评估了常规剂量CD20单抗(利妥昔单抗[R]或奥法木单抗)+减量化疗(环磷酰胺、阿霉素、长春新碱和泼尼松,简称mini-CHOP)的治疗作用,结果显示该方案对≥80岁患者的疗效和安全性均可接受,2年总生存(OS)率59%~65%,毒性可控,多数不良事件发生在治疗前2个周期,包含短疗程长春新碱和强的松的预处理可改善虚弱患者的预后。
高龄患者并没有特定的DLBCL组织学亚型,目前公认的仍是生发中心B细胞样(GCB)和活化B细胞样(ABC)二种亚型,老年患者的ABC亚型发生率增加,目前已提出多种治疗策略以减少ABC DLBCL亚型的不良结果。来那度胺是一种口服免疫调节剂,对B细胞淋巴瘤有多种复杂的免疫活性和抗增殖活性。ABC DLBCL移植瘤模型显示,来那度胺的治疗活性主要是通过抑制IRF4和Cereblon蛋白从而下调BCR-NFKB通路实现。研究显示,来那度胺联合R-CHOP(R2-CHOP)毒性可接受,并可减轻非-GCB表型的不良预后。也有研究表明,来那度胺单药治疗对基因表达谱(GEP)定义的ABC患者有更为明显的临床获益。
研究方法
≥80岁新诊断的DLBCL患者随机分入R-miniCHOP21组和R2-miniCHOP21组,治疗6个周期,根据CD10表达和年龄进行分层。所有患者均在第1周期前1周给予长春新碱1mg,泼尼松60mg/m2/天,共7天。R-MiniCHOP中的利妥昔单抗在第1周期为375mg/m2 第1天静注,第2~6周期1400mg第1天皮下注射,阿霉素25mg/m2第1天,环磷酰胺400mg/m2第1天,长春新碱1mg第1天,强的松40mg/m2第1~5天。来那度胺10mg第1~14天(阿司匹林或低分子肝素预防静脉血栓形成)。主要终点是总生存(OS)。
研究结果
共249例新诊断DLBCL患者随机分组(127例R-miniCHOP,122例R2-miniCHOP)。中位年龄83岁(80-96岁),55%患者为非GCB,二组给药剂量相似。中位随访25.1个月,意向治疗人群的结果分析显示,R2-miniCHOP并没有改善所有患者或非GCB患者的OS(2年OS率,R-miniCHOP为66%,R2-miniCHOP为65.7%,P=0.98)(图1)。53%的R-miniCHOP患者和81%的R2-miniCHOP患者发生了3-4级不良事件。
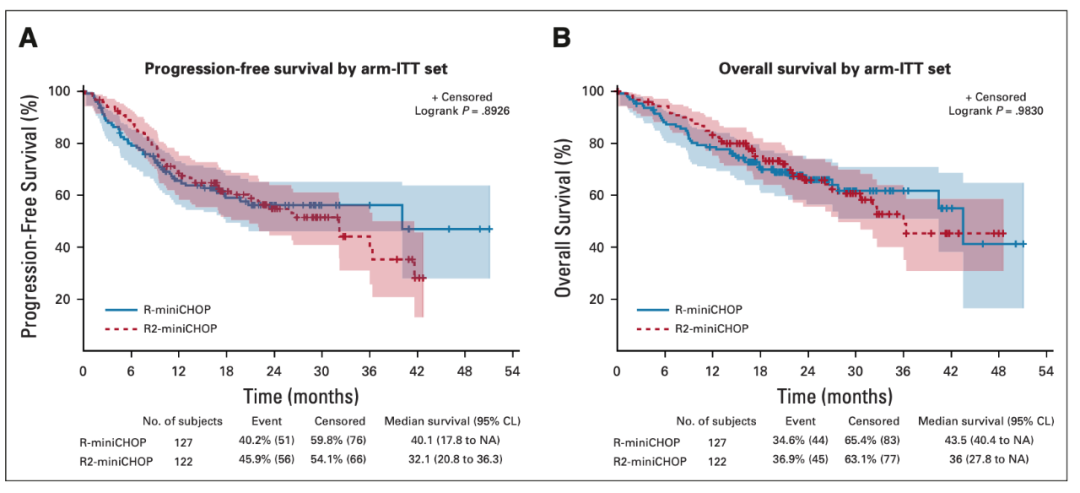
图1 意向性治疗人群的PFS(A)和OS(B)
讨论
这项研究是首次针对年龄超过80岁DLBCL患者的随机III期研究,该研究证明大规模前瞻性研究对这类患者具有可行性。研究还显示,与R-miniCHOP组相比,R2-miniCHOP组患者并无生存优势。中位随访25个月,R-miniCHOP组的2年OS率 66%,与LYSA研究03-7B(59%,95% CI,49~67)和09-7B(65.7%,95% CI,55~73)的结果相似。
这项研究未能得出阳性结果,原因考虑如下:治疗方案不充分,来那度胺剂量不足,然而这项研究中采用10mg剂量时就已出现较多毒性,更高剂量患者可能无法耐受。其他研究中的治疗方案各有不同,但患者均较年轻。ABC DLBCL的III期ROBUST研究(中位年龄65岁)中,来那度胺15mg第1~15天联合标准R-CHOP(225mg/周期)治疗,II期随机ECOG-ACRIN研究(E1412)中DLBCL患者(中位年龄66岁[24~92])采用来那度胺25mg/天第1~10天(250mg/周期)治疗。与这项研究相同,ROBUST研究没能证明ABC DLBCL使用来那度胺联合R-CHOP治疗更有优势,该研究未达到主要研究终点,即R2-CHOP的PFS优于R-CHOP的PFS。相反,ECOG-ACRIN研究的初步结果表明,R2-CHOP组的PFS更优,但二组的≥3级毒性显著不同。这项研究发现,来那度胺的计划用量随治疗进行而显著减少,表明ITT分析中的大部分患者都没能使用充足剂量的来那度胺进行治疗。根据上述数据,这项研究中的治疗策略无法为患者提供更充足的来那度胺用量。另有REMARC研究探索了在R-CHOP后使用来那度胺维持治疗的策略,但60~80岁患者仍未能显示有OS改善。
R2-miniCHOP的毒性可能会严重影响研究的最终结果。事实上,采用X和R-CHOP全量或减量联合治疗策略时,毒性是治疗的主要障碍,尤其是老年患者。比较R-CHOP和R-CHOP+伊布替尼的Phoenix研究中,只有<60岁患者可观察到加用伊布替尼的优势。Phoenix研究中,R-CHOP+伊布替尼治疗老年患者时R-CHOP的剂量强度下降,这可能是联合治疗缺少获益的原因。这项研究中,即使二组的R-miniCHOP剂量强度相等,但高毒性和并发症可能抵消了治疗的获益。皮下注射利妥昔单抗不是导致R2-miniCHOP高频率发生不良事件的原因,既往研究已证实了皮下利妥昔单抗在高龄患者中的安全性和有效性。
这项研究的阴性结果也可能是由于这项研究中ABC DLBCL亚型所占比例明显低于预期,通常认为来那度胺对ABC DLBCL特别有效,因此ABC DLBCL患者数量太少可能无法证实R2-miniCHOP的生存优势。
二项孤立II期研究的合并报道中,R2-CHOP21治疗DLBCL的长期随访结果显示,112例患者,中位年龄69,中位随访5.1年。治疗相关急性白血病和/或骨髓增生异常综合征5年累积发生率0.9%,其他肿瘤为5.4%。这项研究中,随访时间较短为25个月,二组患者的继发恶性肿瘤数量相似(标准组8例,研究组11例),但似乎在质量上有所不同。
提高治疗的有效性和患者生存仍是≥80岁DLBCL的一大挑战。这项研究强调并证实了一些预后因素可用以识别部分标准免疫化疗仍疗效不佳的患者。这些因素中,白蛋白和分期最重要,不依赖于IPI、MNA评分或IADL评分。这个结果证实了LYSA研究037B的结果,表明应这些参数改变高危患者的治疗策略,发展非化疗治疗策略。
总之,这项研究表明,≥80岁新诊断DLBCL患者,不论GCB/ABC状态,在R-miniCHOP中添加来那度胺并不改善OS,还会导致更多不良事件。这项研究再次证实,高龄患者皮下注射利妥昔单抗安全且耐受性良好,与R-miniCHOP的历史数据类似;R-miniCHOP的2年OS率59%~66%,高龄DLBCL患者需要新的治疗策略来改善结果。
参考文献
Oberic L, Peyrade F, Puyade M, et al. Subcutaneous Rituximab-MiniCHOP Compared With Subcutaneous Rituximab-MiniCHOP Plus Lenalidomide in Diffuse Large B-Cell Lymphoma for Patients Age 80 Years or Older. J Clin Oncol. 2021;39(11):1203-1213. doi:10.1200/JCO.20.02666
