从遗传易感基因 看造血干细胞移植治疗预后!
一些与血液或免疫系统疾病相关的基因变异可能会对Allo-HSCT的结果产生影响。2020年12月6日,第62届美国血液学会年会(ASH 2020)召开期间,高博医学(血液病)北京研究中心北京博仁医院吴彤主任团队李智慧医生口头汇报了团队探讨血液肿瘤患者具有的遗传和获得性血液或免疫系统疾病相关的基因变异对Allo-HSCT结果的影响。医学界血液频道特邀吴彤主任和李智慧医生分享该研究的精彩内容!
医学界:您团队针对血液或免疫系统疾病相关的基因变异对血液肿瘤患者Allo-HSCT结果影响的临床研究数据即将在12月6日的ASH上展示。您可否简单介绍下该研究的主要内容?
患者的遗传易感基因变异对Allo-HSCT的影响
吴彤教授:目前,Allo-HSCT已经是血液科的常规治疗方法,它可以使很多疾病得到治愈,但移植之后,可能会出现一些合并症,主要包括移植物抗宿主病(GVHD)、感染、复发等。采用同样的移植方案,为什么不同患者发生合并症的几率及严重程度差异那么大呢?我们想探究这其中的原因,究竟哪些因素会影响Allo-HSCT合并症的发生。移植前将患者及其父母、可能做供者的兄弟姐妹或子女的血样进行基因测序及家系分析,结果发现患者具有的某些免疫缺陷相关的基因变异显著增加了移植后的复发风险。患者具有家族性噬血(HLH)基因和/或范可尼贫血(FA)基因变异明显增加了急性GVHD(aGVHD)和感染的风险。某些肿瘤细胞的基因变异也是移植后复发的高危因素。
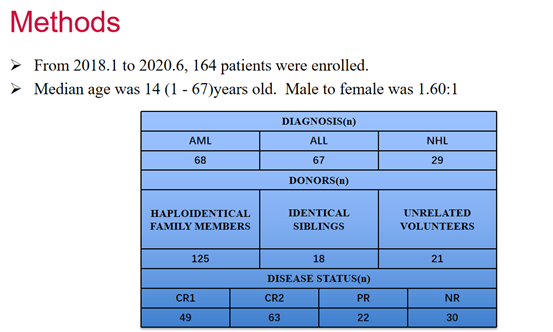
研究方法
李智慧教授:血液系统肿瘤的发生与遗传易感性和外界环境密切相关。目前越来越多地认识到遗传易感基因在恶性血液病的发生发展中都起着重要的作用。2016年WHO年已将髓系肿瘤的胚系易感性纳入对髓系肿瘤和急性白血病分类中。因此,我们研究的目的在于探讨血液肿瘤患者携带的血液和免疫系统疾病相关遗传易感基因与Allo-HSCT的主要并发症,如感染、GVHD以及复发是否具有相关性。
吴彤教授:该研究的临床意义在于发现哪些遗传易感基因的变异容易导致Allo-HSCT合并症的发生,通过患者遗传易感基因的变异情况预判容易出现的合并症种类,并据此制定或调整患者的移植方案,以尽量规避移植后合并症的发生,从而提高Allo-HSCT的安全性及无病生存率。
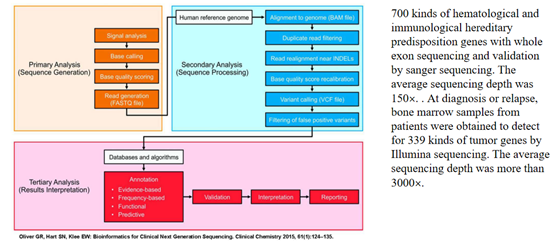
研究设计
李智慧教授:研究发现164例患者共携带191种免疫缺陷相关的遗传易感基因(平均每个患者携带3.5个基因变异;范围0-10)。有26个免疫缺陷相关的遗传易感基因变异出现频率超过6次:TYK2,IFIH1,CFTR,LRBA,IL7R,POLE,RNF31,NLRP12,TTC7A,ATM,CARD14,CHD7,NOD2,TNFRSF13B,BLB,CFB,EPG5,C8A,C8B,CFH,IRF,MSH6,NCF2,NFAT5,PMS2和ST1M1。这些基因的功能包括补体缺陷、固有/先天免疫缺陷、联合免疫缺陷、抗体缺陷、细胞及体液免疫缺陷、先天性吞噬细胞数量或功能缺陷、自身免疫性疾病及免疫失调。
李智慧教授:在26个免疫缺陷相关的遗传易感基因中,IFIH1和IL10RB基因变异是移植后复发的不良预后因素(P=0.006,P=0.007)。
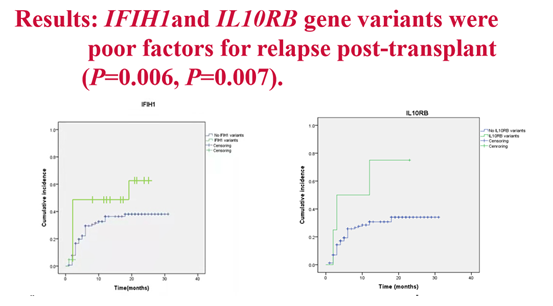
IFIH1和IL10RB基因变异是移植后复发的不良预后因素
与没有HLH、FA相关基因变异的患者相比,具有HLH和/或FA相关基因变异的患者aGVHD和/或感染的发生率显著增高(p=0.019)。
在164例患者中发现153种肿瘤基因变异(平均每个患者携带1.93个基因变异;范围0-15)。其中17种肿瘤基因变异出现频率超过4次:TP53,PTPN11,KIT,FLT3,NRAS,NUDT15,STK11,CREBBP,NPM1,DNAH9,DNMT3A,IDH2,HEK2,KRAS,KMT2C,NOTCH1和NR3C1。这些突变涉及的通路有TCA循环、DNA甲基化、ATP酶活性、Notch信号、代谢调节、表观遗传、信号通路、细胞周期。其中TP53,KRAS和NUDT15基因变异是Allo-HSCT后复发的不良因素(P=0.000025,P=0.0082,P=0.000018)。
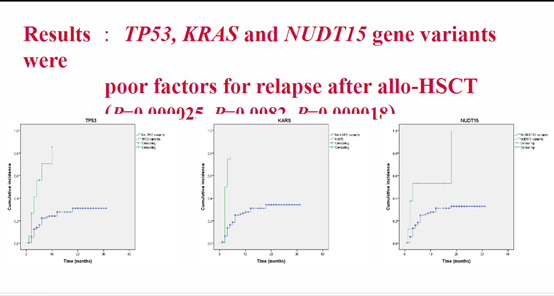
TP53,KRAS和NUDT15基因变异是Allo-HSCT后复发的不良因素
分析供者遗传易感基因变异的重要性
吴彤教授:基因检测可以帮助我们解读很多信息,就该研究而言,我们可以更好地预测哪些患者容易出现合并症?容易出现哪些合并症?医生应该重点采取哪些针对性的策略来预防或减少这些合并症的发生。将来我们也会进一步做供者携带的遗传易感基因变异对Allo-HSCT结果影响的研究。
目前,我们已经用血液和免疫系统疾病相关遗传易感基因变异的筛查实验来帮助选择供者,当患者需要移植的时候,从配型角度家属中可能有几个人都可以做供者,但究竟谁是最理想的供者呢?除了HLA配型因素以外,还要分析遗传背景,再结合造血及免疫功能的检查,从而确定最佳供者。供者选对了,对增加移植的成功率至关重要。
究竟谁需要做遗传易感基因检测?
吴彤教授:对所有准备移植的患者,都建议进行遗传易感基因的检测。我们曾经收治了一些外院移植后发生严重合并症且治疗特别困难的患者。我们对这些患者和其供者进行了遗传易感基因的检测,结果发现某些供者就携带多种免疫缺陷基因,最终导致患者移植后发生严重的病毒感染,控制难度大,且也增加了移植后疾病复发的风险。当我们给供者做了遗传易感基因的检测后,就可以尽可能地避免此类问题的发生。
李智慧教授:难治复发的恶性血液肿瘤患者,没有非血缘供者准备行亲缘移植的都需要做遗传易感基因的检测。目前临床上对于遗传易感基因的检测并不足够,例如外院移植后三个月血液学复发的B-ALL患者,通过我院700+种遗传易感基因的检测,发现该患者第一次移植的同胞全合供者携带6个免疫缺陷相关的遗传易感基因,说明供者的免疫原性较弱,这可能就是患者移植后早期血液学复发的主要原因。在该患者行二次移植时,我们谨慎的选择了非血缘供者,目前该患者二次移植后一年半,MRD阴性,分子生物学水平完全缓解。
遗传易感基因检测是否要纳入移植程序中的常规项目?
吴彤教授:目前,越来越多的报道认为遗传易感基因的变异不仅容易导致髓系肿瘤,也容易导致淋巴系统肿瘤和实体瘤,因此我们才建立了此筛查试验。除了诊断以外,遗传易感基因检测也可以帮助医生判断患者是否容易被化疗治愈,缓解后的治疗应如何选择。
该研究目前还处于探索阶段,遗传易感基因检测要不要作为移植前的常规检测项目,可能还需要一段时间的检验。初步的研究结果对临床医生的工作还是具有一定的指导意义的,患者也可以通过此项基因检测获益。


