治愈急性早幼粒细胞白血病,更需规范化分层诊疗
急性早幼粒细胞白血病(acute promyelocytic leukemia,APL)是急性髓系白血病(AML)中的一种亚型,骨髓中以多颗粒的早幼粒细胞为主,是一类以急性出血为主要临床特征的白血病,死亡率较高,被认为是最凶险的白血病亚型。
随着全反式维甲酸(ATRA)和砷剂(ATO)的应用,APL患者早期死亡率明显下降,目前APL治愈率可达到95%。权威指南《美国国立综合癌症网络(NCCN)肿瘤学临床实践指南:急性髓系白血病》已更新到2021.V3版本,今天跟着小编一起来学习吧!
01 发病机制和临床特点
绝大多数APL患者具有特异性染色体易位t(15;17)(q22;q12),形成PML-RARα融合基因,其蛋白产物导致细胞分化阻滞和凋亡不足,是APL发生的主要分子机制。APL易见于中青年人,平均发病年龄为44,APL占同期AML的10%-15%,发病率约0.23/10万。
APL临床表现凶险,典型表现为出血、发热、骨关节疼痛、感染以及肝脾等器官浸润,起病及诱导治疗过程中容易发生出血和栓塞而引起死亡。由于ATRA及ATO的规范化临床应用,APL已成为基本不用进行造血干细胞移植即可治愈的白血病。
02 实验室检查和诊断
表1 APL患者的检查

表2 APL患者的诊断

03 治疗
▌ 低危患者的治疗
ATRA+ATO方案为低危患者的标准诱导治疗方案,后进行巩固治疗(约半年)和维持治疗(两年),具体方案如图1。
▌ 高危患者的治疗
对于伴有心脏基础病的患者,诱导方案多为ATRA联合单抗或其他非蒽环类化疗药物。对于不伴有心脏基础疾病的高危患者,诱导方案多为ATRA联合蒽环类药物。在巩固治疗阶段多使用阿糖胞苷进行化疗,给予腰穿鞘注预防中枢神经系统白血病,后进行两年的维持治疗,具体方案如图1。
▌ 二线治疗
一般采用砷剂±ATRA±蒽环类化疗进行再次诱导治疗。诱导缓解后必须进行鞘内注射,预防中枢神经系统白血病。达再次缓解(细胞形态学)者进行PML-RARα融合基因检测,融合基因阴性者行自体造血干细胞移植或砷剂巩固治疗(不适合移植者)6个疗程,融合基因阳性者进入临床试验或行异基因造血干细胞移植。再诱导未缓解者可加入临床研究或行异基因造血干细胞移植。
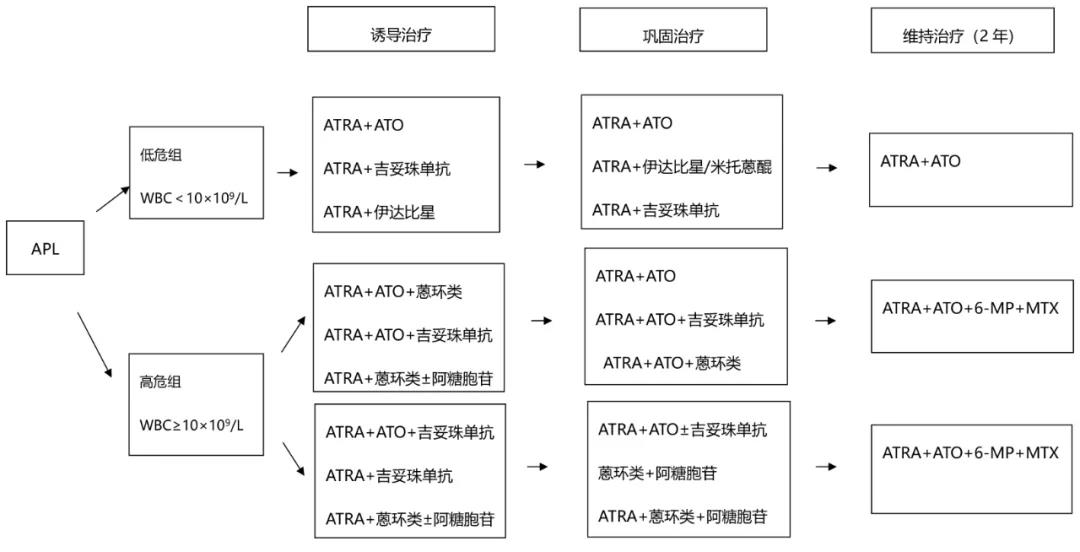
图1 APL患者的临床路径
04 疗效评估
▌ 诱导阶段评估
ATRA的诱导分化作用可以持续较长时间,骨髓形态学评价一般在诱导治疗第4-6周、血细胞计数恢复后进行,此时细胞遗传学一般正常,而PML-RARα或发病时相应异常基因转录本在多数仍为阳性。
▌ 微小残留病(MRD)监测
建议采用定量PCR监测骨髓PML-RARα转录本水平,治疗期间建议2-3个月进行1次分子学反应评估,持续监测2年。上述融合基因持续阴性者继续维持治疗,融合基因阳性者4周内复查。复查阴性者继续维持治疗,确实阳性者按复发处理。流式细胞术因对于APL的MRD敏感性显著小于定量PCR,因此不建议单纯采用流式细胞术对APL进行MRD监测。
小结:
本版指南较2020.V4版指南更新内容较少,从新版指南可以看出,随着ATRA的发现以及ATO的引入及对PML-RARA融合蛋白协同破坏的认识和发展,使直接作用于PML-RARa融合基因的两种靶向药物在APL治疗中取得了无与伦比的成功,APL患者的完全缓解率达到85%-90%,已经成为唯一一种能够治愈的AML亚型,同时也是第一个通过诱导分化和针对肿瘤细胞分子靶向治疗的恶性血液肿瘤。随着对APL认识的加深与治疗方案的发展,分层治疗方案更有利于APL的治疗,对于高危APL患者的治疗方案仍需要进一步优化。
参考文献:
[1]2021.V3版《NCCN肿瘤学临床实践指南:急性髓系白血病》
