整合素,全面促进肿瘤进展的免疫分子
在多细胞生物体中,细胞与周围细胞外基质(ECM)的相互作用,对组织的生理学和完整性至关重要。在哺乳动物细胞中,整合素是主要的ECM受体,提供外部基质支架和内部肌节蛋白细胞质之间的联系。
18个α整合素亚基和8个β整合素亚基以不同的组合组装,形成24个跨膜异二聚体,具有对不同配体的结合特异性。整合素受体在转录和翻译水平上以组织特异性的方式进行调控。此外,从质膜上进行的内质体来回转运、表面极化分布和ECM接触位点的动态定位都是整合素介导的粘附的关键调控步骤。
整合素的功能在许多病理环境中被破坏,如癌症。事实上,细胞粘附和转移的改变几乎参与到癌症进展的每一个阶段,从肿瘤开始到转移。
整合素参与肿瘤进展
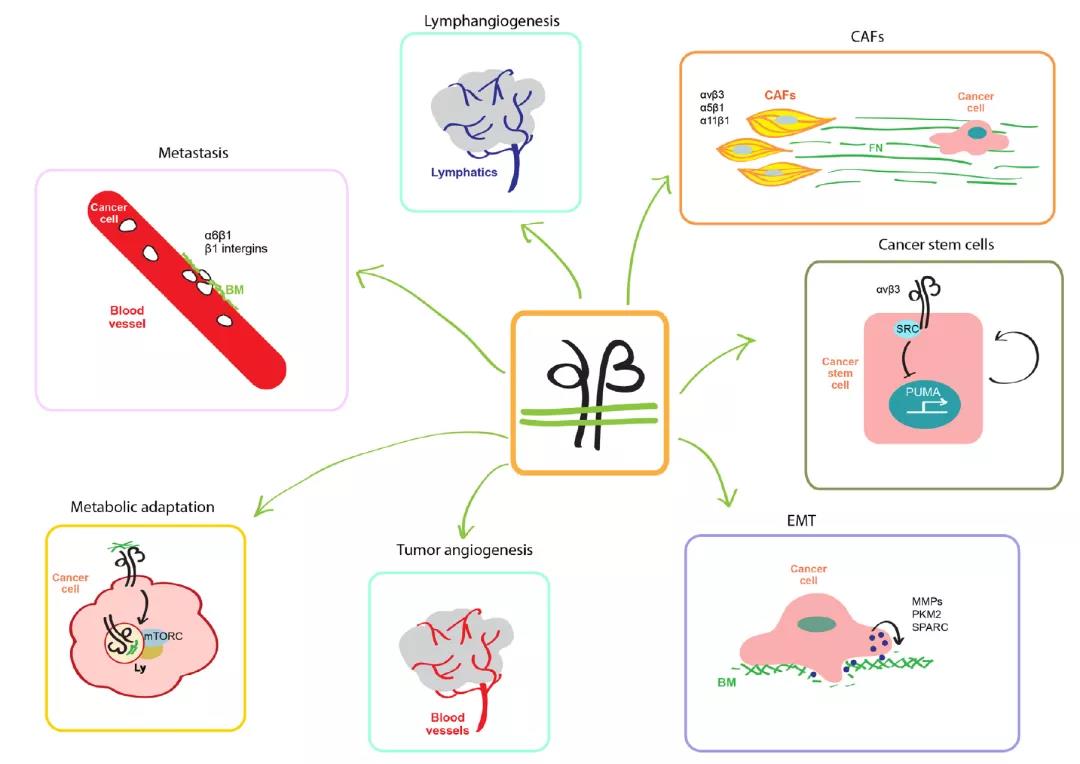
- 整合素和细胞外基质调节癌细胞的代谢行为和溶酶体上的mTORC激活。
- 整合素促进了新的血管和淋巴管的形成,以支持肿瘤的生长、侵袭和转移遗传。
- 在上皮到间充质转化(EMT)过程中,整合素维持着癌细胞的迁移表型,以基质金属蛋白酶(MMPs)、丙酮酸激酶(PKM2)的M2亚型和基质细胞蛋白SPARC的分泌增加为特征。
- 在乳腺癌中,αvβ3整合素可以诱导促凋亡基因PUMA的转录,从而支持肿瘤细胞的干性。
- 在肿瘤微环境中,整合素α5β1产生和聚合大量CAFs,形成纤维连接蛋白(FN),癌细胞以αvβ3依赖的方式方向迁移。
- 此外,α11β1整合素和PDGFR-β表达的CAFs,还促进了乳腺癌的进展。整合素介导的与血管基底膜(BM)的层粘连蛋白的相互作用,也促进了癌细胞在远处器官中的转移和定植。
整合素药物开发
整合素是非常有吸引力的靶点,理论上可以阻止癌症进展的几个关键过程,如细胞增殖、生存和迁移。然而,尽管临床前研究的初步结果令人鼓舞,但是单克隆抗体、拮抗肽和作为整合素功能抑制剂的小分子(如下表),在临床试验中基本上不成功,迄今为止还没有发现该类靶点临床有效的抗癌药物。
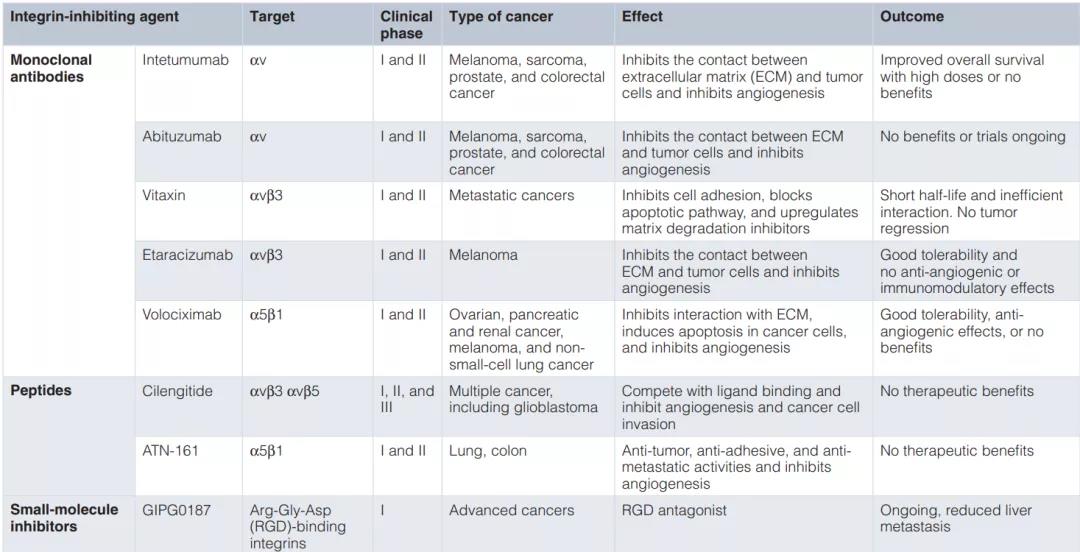
虽然许多整合素αβ异二聚体与肿瘤的发展有关,但其中只有少数在临床试验中被用作治疗靶点。传统的抑制整合素的抗癌药物已经被认为是破坏了配体结合的能力。然而,当与高亲和力药物结合时,整合素仍然可以激活细胞内信号,促进细胞在ECM分离条件下的生存(抗体无法完全阻断信号传导)。
虽然大多数整合素抑制剂主要用于单药抗血管生成治疗,但除血管以外还有其他肿瘤微环境成分(如浸润免疫抑制细胞,CAFs等),整合素抑制可能改善癌症定向免疫反应,而CAFs可作为整合素治疗的新靶点。例如,通过破坏单核细胞对血管内皮的黏附,并促进外渗进入肿瘤组织。发现α4β1整合素拮抗剂会阻碍了肿瘤的巨噬细胞定植和血管生成。此外,靶向αv和β1整合素亚基会阻碍ECM的沉积和CAFs的重塑,最终降低了癌症的侵袭性。αvβ6整合素的表达在结肠、肺、乳房、宫颈、卵巢/输卵管、胰腺和头颈等实体肿瘤,而在成人上皮组织上没有,使这种受体成为免疫治疗策略的重要靶点(肿瘤微环境复杂的成分,联合疗法可能是出路)。
提高整合素靶向治疗影响的进一步策略是发现新的合适的生物标记,用于成功选择从这类药物治疗中获益更多的患者(合适标志物筛选合适的病人)。
小编总结
最近的几项研究提供了关于整合素、其上游调制剂、下游效应子参与的,不同类型癌症中标准护理治疗的发展、进展和耐药性的证据。除了影响细胞粘附、运动性、侵袭和转移性遗传外,整合素还被报告对癌细胞的干性、无锚固的生长、代谢有影响。使用整合素抑制作为单种抗癌药物的众多临床试验令人失望,未来的临床开发更加会倾向于联合治疗。
事实上,可能由于整合素与其他几个受体系统(例如,生长因子和G蛋白偶联受体)、代谢通路、损伤修复通路相互作用,它们的药理抑制可能在挽救癌症对化疗、靶向治疗和放疗的耐药性方面有效。进一步全面描述整合素控制癌细胞行为的分子和细胞机制,产生一套更有效的策略,在抗癌治疗中充分利用整合素抑制。
参考文献
1.Sun Z, Costell M, Fässler R: 整联蛋白 activation by talin, kindlin and mechanical forces. Nat Cell Biol. 2019; 21(1): 25–31.
2.Every step of the way: 整联蛋白s in cancer progression and metastasis. Nat Rev Cancer. 2018; 18(9): 533–48
3.Valdembri D and Serini G. The roles of 整联蛋白s in cancer. Faculty Reviews 2021 10:(45)
